普通注射劑無需進行BE試驗,雜質、穩定性、無菌性、包材相容性等方面是研究重點。對于口服制劑而言,一致性評價的重點工作是使仿制藥與原研藥在體內、體外的溶出曲線、速度達到一致,因此需要進行BE試驗。但注射劑藥物通常直接注入血管,除了特殊注射劑(如脂質體、靜脈乳、微球、混懸性注射液、油溶液、膠束等),普通注射劑不存在溶出和吸收的差別,因此不需要進行BE試驗。而由于注射劑藥物直接注入血管,因此注射劑評價的重要內容是對于其安全性的研究,包括在藥品的雜質、穩定性、無菌性和包材的相容性等方面,都需要達到與原研藥同樣的水平。
政策基本完善,注射劑一致性評價有望加速,申報較早、企業較多的品種有望率先通過。注射劑一致性評價的政策已基本完善。鑒于正式的《技術要求》與2019年的征求意見稿之間差異很小,預計多數已在CDE審評的一致性評價申請(包括存量補充申請+新分類申報)大概率符合相關技術要求,隨著審評審批的推進,有望快速通過。其中,申報較早的品種按照審評隊列優先順序有望率先通過,但不排除部分申報較早的品種由于技術要求的更新而需補充材料的可能性;申報企業較多的品種可能隨著評審人員對其關鍵技術指標的熟悉掌握而有可能率先通過;其中技術能力強、質量控制好的企業有望一馬當先。
2020年5月14日,國家藥監局發布《關于開展化學藥品注射劑仿制藥質量和療效一致性評價工作的公告(2020年第62號)》,明確:已上市的化學藥品注射劑仿制藥,未按照與原研藥品質量和療效一致原則審批的品種均需開展一致性評價。藥品上市許可持有人應當依據國家藥品監督管理局發布的《仿制藥參比制劑目錄》選擇參比制劑,并開展一致性評價研發申報。2020年5月14日,國家藥品監督管理局藥品審評中心發布《化學藥品注射劑仿制藥質量和療效一致性評價技術要求》《化學藥品注射劑仿制藥質量和療效一致性評價申報資料要求》《化學藥品注射劑(特殊注射劑)仿制藥質量和療效一致性評價技術要求》
仿制藥一致性評價政策
發文時間 | 發文部門 | 發文時間 | 發文部門 | 主要內容 |
2016.05.26 | 國家食品藥品監督管理局 | 《關于落實〈國務院辦公廳關于開展仿制藥質量和療效一致性評價的意見〉有關事項的公告》 | 國食藥監[2016]106號 | 對一致性評價的藥品目錄,研究內容,程序等相關內容進行了規定,進一步推進藥品一致性評價。 |
2016.07.01 | 國家食品藥品監督管理局 | 《關于研制過程中所需研究用對照藥品一次性進口有關事宜的意見》 | 國食藥監[2016]120號 | 對于已在中國境外上市但尚未在中國境內批準上市的藥品的進口申報和申報內容進行了規定。 |
2016.08.17 | 國家食品藥品監督管理局 | 《化學藥品仿制藥口服固體制劑質量和療效一致性評價申報資料要求(試行)》 | 國食藥監[2016]120號 | 對化學藥品仿制藥口服固體制劑質量和療效一致性評價的申報材料和內容進行了規定。 |
2017.02.07 | 國家食品藥品監督管理局 | 《仿制藥質量和療效一致性評價臨床有效性試驗一般考慮》 | 國食藥監[2017]18號 | 對于找不到或無法確定參比制劑的,需開展臨床有效性試驗的仿制藥一致性評價的方法進行了規定。 |
2017.02.17 | 國家食品藥品監督管理局 | 《仿制藥質量和療效一致性評價工作中改規格藥品(口服固體制劑)評價一般考慮》《仿制藥質量和療效一致性評價工作中改劑型藥品(口服固體制劑)評價一般考慮》《仿制藥質量和療效一致性評價工作中改鹽基藥品評價一般考慮》 | 國食藥監[2017]27號 | 對于口服固體制劑中改規格,改劑型和改鹽基這三類藥品的一致性評價的的方法進行了規定。 |
2017.04.05 | 國家食品藥品監督管理局 | 《仿制藥質量和療效一致性評價品種分類指導意見》 | 國食藥監[2017]49號 | 為了推動仿制藥質量和療效一致性評價,對藥品的品種進行了分類。 |
2017.05.18 | 國家食品藥品監督管理局 | 《仿制藥質量和療效一致性評價研究現場核查指導原則》《仿制藥質量和療效一致性評價生產現場檢查指導原則》《仿制藥質量和療效一致性評價臨床試驗數據核查指導原則》《仿制藥質量和療效一致性評價有因檢查指導原則》 | 國食藥監[2017]77號 | 對于仿制藥質量和療效一致性評價中研究現場核查的各個方面內容進行了規定。 |
2017.08.25 | 國家食品藥品監督管理局 | 《關于仿制藥質量和療效一致性評價工作有關事項的公告》 | 國食藥監[2017]100號 | 對一致性評價工作各環節進行了優化調整。 |
2017.10.08 | 中共中央辦公廳,國務院辦公廳 | 《關于深化審評審批制度改革鼓勵藥品醫療器械創新的意見》 | 廳字(2017)42號 | 提出深化改革審評審批制度,鼓勵藥品醫療器械創新。 |
數據來源:公開資料整理
2019年6月13日,仿制藥參比制劑目錄第二十一批(2019年第34號)公布,首次加入了注射劑。其中一共233個產品,注射劑有163個,共計69個注射劑藥品種類。注射劑參比制劑來源情況只包含兩類,其中國內上市的原研藥品占比69%。2019年8月27日,仿制藥參比制劑目錄第二十二批中一共507個產品(2019年第56號),注射劑有239個,共計84個注射劑藥品種類。與第二十一批不同的是,未進口藥品作為參比制劑占大多數,為65%,國內上市的原研藥品23%。此后,CDE又陸續公布了六批含注射劑品種的參比制劑目錄。目前八批參比制劑目錄共計包含855個注射劑參比制劑,預計已相對齊全。
第二十一批參比制劑制劑來源分布
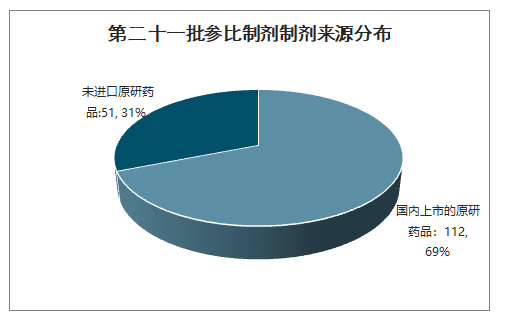
數據來源:國家食品藥品監督管理局局官網、智研咨詢整理
第二十二批參比制劑制劑來源分布

數據來源:國家食品藥品監督管理局局官網、智研咨詢整理
智研咨詢發布的《2020-2026年中國注射劑行業市場營銷模式及投資規劃分析報告》數據顯示:截止2020年5月17日,CDE共已受理1324個注射劑一致性評價,其中已有43個申請(視同)通過一致性評價,86個申請審評結束但暫未明確結論,1195個申請正在審評審批中。1195個正在審評審批的申請中,683個為存量注射劑品種的一致性評價補充申請,512個為按照新注冊分類標準申報的上市申請。
已有43個注射劑品規(視同)通過一致性評價
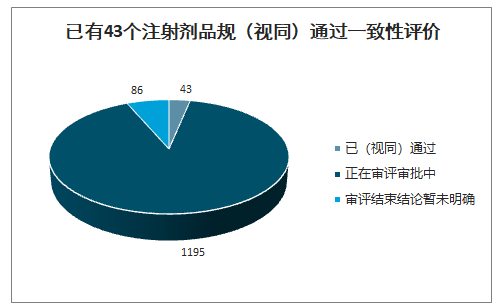
數據來源:公開資料整理
正在審評審批的大多為存量品種的一致性評價申請
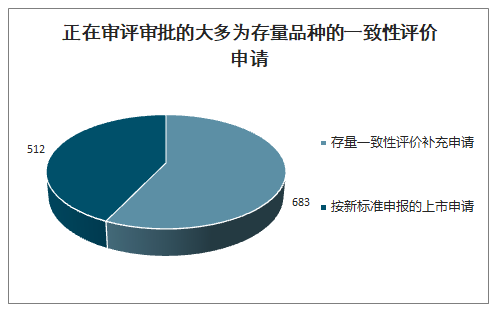
數據來源:公開資料整理
截至2020年5月17日,注射劑一致性評價,通過企業數量最多的品種為布洛芬、鹽酸阿芬太尼、左乙拉西坦注射液等,通過品種數量最多的企業包括四川匯宇、恒瑞醫藥、人福藥業、大冢制藥等。目前已經通過的品種主要為按照新3/4類申報生產后獲批的注射劑,上市后視同通過一致性評價。同時,少量產品通過補充申請的路徑獲批,但均是在海外上市、海內外共線的品種。
已(視同)通過注射劑一致性評價企業最多的品種統計

數據來源:公開資料整理
(視同)通過注射劑一致性評價品種最多的企業統計
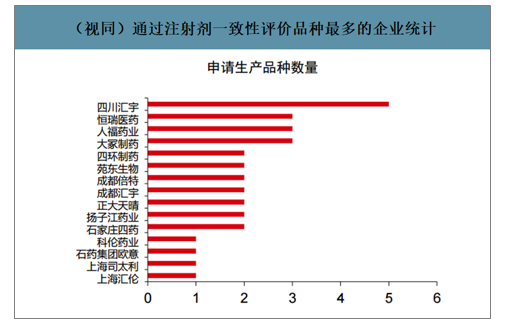
數據來源:公開資料整理
已(視同)申請注射劑一致性評價企業最多的品種統計
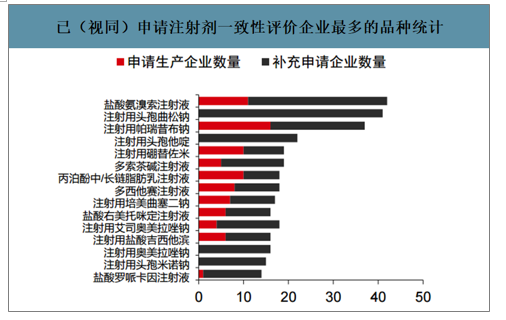
數據來源:公開資料整理
(視同)申請注射劑一致性評價品種最多的企業統計
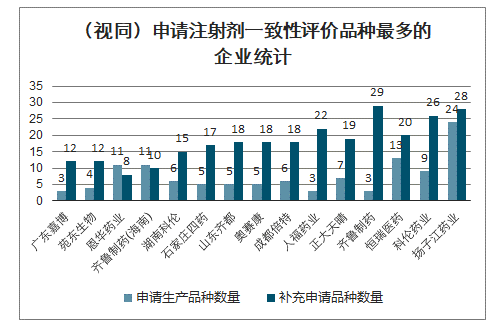
數據來源:公開資料整理
各疾病領域樣本醫院注射劑金額及占所有劑型比例

數據來源:公開資料整理
 智研咨詢 - 精品報告
智研咨詢 - 精品報告

2026-2032年中國注射劑行業發展動態及投資規劃分析報告
《2026-2032年中國注射劑行業發展動態及投資規劃分析報告》共八章,包含新型注射液行業營銷模式及策略分析,中國注射劑領先企業案例分析,注射劑行業前景預測與投資建議等內容。

 公眾號
公眾號
 小程序
小程序
 微信咨詢
微信咨詢






















![國家對注射劑行業監管日益加強,生物藥注射劑行業將成市場發展熱點[圖]](http://img.chyxx.com/2021/03/20210323134620.jpg?x-oss-process=style/w320)
