1、新冠病毒傳播力強,多國強力隔離防控
截至2020年4日7日,全球累計新冠確診病例超140萬例,4月7日單日新增超8萬例。由于新冠病毒感染者中約80%為輕癥患者或無癥狀感染者,若不采取強力社會隔離措施,極難控制其傳播。在巨大的防疫壓力下,多國出臺了強力居家隔離和邊境管制措施。意大利、西班牙、法國等歐盟國家相繼實施了全國封鎖;英國要求全民居家隔離;美國宣布入境禁令,多州發布“居家令”;日本包括東京在內的7個都府縣亦于4月7日進入緊急狀態,要求居民盡量避免外出。我國雖前期國內防疫措施取得階段性成果,但現依然存在“防輸入”壓力,當前處于“外國公民入境暫停、本國公民入境隔離”的強力邊境管控之中。
全球新冠累計確診和新增確診病例數
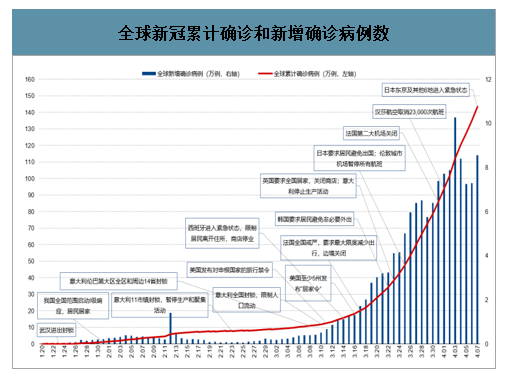
數據來源:公開資料整理
2、新型冠狀病毒檢測方法
新型冠狀病毒的檢測方法主要包含核酸檢測、抗體檢測、抗原檢測幾種方法。由于抗原檢測檢出率較低,目前新冠檢測主要集中在抗體和核酸檢測。核酸檢測目前是新型冠狀病毒檢測的“金標準”,具有早期診斷、靈敏度和特異性高等特點;但抗體檢測操作便捷、檢測迅速,可作為核酸診斷的補充手段。
3、新冠檢測試劑盒國內外上市情況
1)國內外審評要求
2020年3月以來,新冠肺炎全球爆發,為應對緊張的疫情,國家藥品監督管理局(NMPA)、美國食品藥品監督管理局(FDA)、世界衛生組織(WHO)開放了應急審批通道,加快了新型冠狀病毒檢測試劑盒的審批。
監管機構對新冠病毒核酸檢測試劑發布審評標準時間表
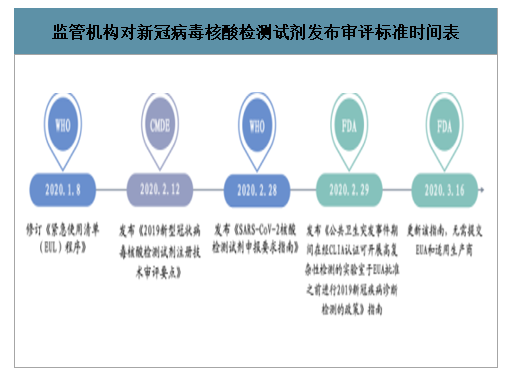
數據來源:公開資料整理
智研咨詢發布的《2020-2026年中國新冠檢測試劑盒產業運營現狀及發展前景分析報告》數據顯示:2020年2月28日,美國微生物學會(theAmericanSocietyofMicrobiology,ASM)致函FDA,對在新冠肺炎爆發期間,通過緊急使用授權(emergencyuseauthorizationEUA)流程可能對供臨床實驗室用的診斷檢測的影響表示擔憂。一天后,FDA發布即時生效的指南,允許某些實驗室在獲得EUA授權之前使用實驗室開發的檢測(laboratorydevelopedtest,LDT)。
FDA在3月16日更新后的指南中表示,商業制造商可以開發新冠病毒檢測,在提交EUA請求之前的15個工作日內,一旦通過驗證,就可以開始使用相關的檢測。制造商可以提供檢測的使用說明,并在其網站公布檢測性能信息。FDA同時通過沒有緊急使用授權的情況下,準許使用血清學檢測,但要求在檢測中包括警告聲明,注明“FDA指出,該測試尚未得到FDA審評,抗體檢測的結果不應作為診斷或排除新冠病毒感染,或告知感染狀況的唯一依據。”
通過對比中國CMDE、美國FDA以及WHO對于新冠檢測試劑盒的注冊審評要求,總體來說,中國的審評要求更加嚴格,對于細節的要求比較充分和明確。同時,明確的具體要求也有利于申請人在產品確認過程中一步到位,但國際監管機構也有部分先進的經驗值得我國學習。
CMDE、WHO及FDA新型冠狀病毒核酸檢測試劑審評要求對比
CMDE、WHO及FDA新型冠狀病毒核酸檢測試劑審評要求對比 | |||
項目 | 中國 | WHO | FDA |
文件適用范圍 | 中國IVD生產企業;產品在境內上市 | 全球企業;全球采購 | 經CLIA認證的實驗室;商業生產商 |
質量管理體系 | 與WHO類似 | EUR程序(質量管理體系審查+上市后監管) | 未提及 |
應急審評產品證據 | 認可有限性證據 | 產品描述信息以及安全有效性證據 | 有效性證據水平為“可能有效” |
產品質量控制要求 | 明確主要原材料的驗證過程和質量控制標準;要求試劑盒中具備質控體系 | 簡單描述申報產品的原材料/成分信息;未對試劑盒中的質控體系進行要求 | 未對試劑盒中的質控體系進行要求 |
性能要求(核酸提取/純化性能;病毒樣本包容性驗證;精密度;計量學溯源性;適用機型…) | 明確要求研究配套提取試劑的性能;要求對包容性相關序列分析和試驗驗證;要求精密度驗證的充分性;進行量值研究;要求提供產品說明書-適用機型項中列出所有型號儀器性能評估資料 | 未要求研究配套提取試劑的性能;未要求對包容性相關序列分析和試驗驗證;概括性描述精密度影響因素和樣本濃度水平;進行量值研究;未考慮機型因素 | 未要求研究配套提取試劑的性能;要求對包容性相關序列分析,但未要求試驗驗證;未提及精密度要求;未提及量值研究;可能考慮適用儀器一般是密閉系統,但未提及 |
臨床試驗要求(試驗機構;樣本要求;入組人群;試驗結果統計分析…) | 三家以上機構進行臨床試驗;確診病例不少于200例,排除病例不少于300例;適用人群為新冠肺炎疑似病例;結果挖掘更充分 | 未對試驗機構進行要求;50個前瞻性陽性樣本;入組人群為各類人群;臨床結果僅計算一致性百分比 | 未對試驗機構進行要求;30個反應性人工樣本和30個非反應性樣本;未規定入組人群;臨床結果僅計算一致性百分比 |
數據來源:公開資料整理
2)國內外獲批試劑盒
截至2020年4月26日,國家藥品監督管理局已應急審批30個新型冠狀病毒檢測試劑。其中核酸檢測試劑18個,抗體檢測試劑11個。
國內已批準新型冠狀病毒檢測試劑
國內已批準新型冠狀病毒檢測試劑 | |||||
檢測方法 | 序號 | 注冊證號 | 產品名稱 | 注冊人 | |
核酸檢測 | 熒光PCR法 | 1 | 國械注準20203400057 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法) | 上海之江生物科技股份有限公司 |
2 | 國械注準20203400058 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法) | 上海捷諾生物科技有限公司 | ||
3 | 國械注準20203400060 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法) | 華大生物科技(武漢)有限公司 | ||
4 | 國械注準20203400063 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法) | 中山大學達安基因股份有限公司 | ||
5 | 國械注準20203400064 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法) | 圣湘生物科技股份有限公司 | ||
6 | 國械注準20203400065 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法) | 上海伯杰醫療科技有限公司 | ||
7 | 國械注準20203400179 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法) | 北京卓誠惠生生物科技股份有限公司 | ||
8 | 國械注準20203400184 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法) | 邁克生物股份有限公司 | ||
9 | 國械注準20203400212 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法) | 武漢明德生物科技股份有限公司 | ||
10 | 國械注準20203400299 | 新型冠狀病毒(2019-nCoV)核酸檢測試劑盒(熒光PCR法) | 上海復星長征醫學科學有限公司 | ||
11 | 國械注準20203400322 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法) | 北京金豪制藥股份有限公司 | ||
12 | 國械注準20203400384 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法) | 江蘇碩世生物科技股份有限公司 | ||
恒溫擴增-實時熒光法 | 13 | 國械注準20203400241 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(恒溫擴增-實時熒光法) | 杭州優思達生物技術有限公司 | |
雜交捕獲免疫熒光法 | 14 | 國械注準20203400298 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(雜交捕獲免疫熒光法) | 安邦(廈門)生物科技有限公司 | |
聯合探針錨定聚合測序法 | 15 | 國械注準20203400059 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(聯合探針錨定聚合測序法) | 華大生物科技(武漢)有限公司 | |
恒溫擴增芯片法 | 16 | 國械注準20203400178 | 六項呼吸道病毒核酸檢測試劑盒(恒溫擴增芯片法) | 成都博奧晶芯生物科技有限公司 | |
RNA捕獲探針法 | 17 | 國械注準20203400300 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(RNA捕獲探針法) | 上海仁度生物科技有限公司 | |
RNA恒溫擴增-金探針層析法 | 18 | 國械注準20203400301 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(RNA恒溫擴增-金探針層析法) | 武漢中幟生物科技股份有限公司 | |
雙擴增法 | 19 | 國械注準20203400302 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(雙擴增法) | 武漢中幟生物科技股份有限公司 | |
抗體檢測膠體金法 | 20 | 國械注準20203400176 | 新型冠狀病毒(2019-nCoV)抗體檢測試劑盒(膠體金法) | 廣州萬孚生物技術股份有限公司 | |
21 | 國械注準20203400177 | 新型冠狀病毒(2019-nCoV)IgM/IgG抗體檢測試劑盒(膠體金法) | 英諾特(唐山)生物技術有限公司 | ||
22 | 國械注準20203400199 | 新型冠狀病毒(2019-nCoV)IgM抗體檢測試劑盒(膠體金法) | 廣東和信健康科技有限公司 | ||
23 | 國械注準20203400239 | 新型冠狀病毒(2019-nCoV)IgM/IgG抗體檢測試劑盒(膠體金法) | 南京諾唯贊醫療科技有限公司 | ||
24 | 國械注準20203400240 | 新型冠狀病毒(2019-nCoV)IgM/IgG抗體檢測試劑盒(膠體金法) | 珠海麗珠試劑股份有限公司 | ||
25 | 國械注準20203400367 | 新型冠狀病毒(2019-nCoV)抗體檢測試劑盒(膠體金法) | 上海芯超生物科技有限公司 | ||
磁微粒化學發光法 | 26 | 國械注準20203400182 | 新型冠狀病毒(2019-nCoV)IgM抗體檢測試劑盒(磁微粒化學發光法) | 博奧賽斯(重慶)生物科技有限公司 | |
27 | 國械注準20203400183 | 新型冠狀病毒(2019-nCoV)IgG抗體檢測試劑盒(磁微粒化學發光法) | 博奧賽斯(重慶)生物科技有限公司 | ||
28 | 國械注準20203400198 | 新型冠狀病毒(2019-nCoV)抗體檢測試劑盒(磁微粒化學發光法) | 廈門萬泰凱瑞生物技術有限公司 | ||
29 | 國械注準20203400365 | 新型冠狀病毒(2019-nCoV)IgG抗體檢測試劑盒(磁微粒化學發光法) | 丹娜(天津)生物科技有限公司 | ||
30 | 國械注準20203400366 | 新型冠狀病毒(2019-nCoV)IgM抗體檢測試劑盒(磁微粒化學發光法) | 丹娜(天津)生物科技有限公司 | ||
數據來源:公開資料整理
國外疫情日趨嚴峻,各國陷入試劑盒短缺的困境。國產試劑盒具有先發臨床和成本優勢,多家國內企業開始向世界各國出口試劑盒。3月開始,歐洲嚴峻疫情態勢產生新冠檢測的巨大需求,多家中國企業瞄準了歐洲龐大的新冠檢測市場,并積極推動自主研發的新冠檢測產品進入歐洲市場。截至4月22日,國內從事新冠檢測相關產品研發生產的企業近千家,其中產品已獲得CE認證的企業超過160家。
獲得歐盟CE認證的廠家和產品(不完全統計)
獲得歐盟CE認證的廠家和產品(不完全統計) | |
達安基因 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法) |
丹大生物 | 新型冠狀病毒IgM/IgG快速檢測試劑盒 |
漢唐生物 | 新型冠狀病毒抗體檢測試劑盒(免疫層析法) |
華大基因 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法) |
華邁興微 | 微流控化學發光新冠病毒檢測試劑盒 |
凱普生物 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法) |
邁克生物 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法) |
2019新型冠狀病毒IgM/IgG抗體檢測試劑盒(膠體金法) | |
美康生物 | 新型冠狀病毒COVID-19抗體(IgG/IgM)聯合檢測試劑盒(乳膠法) |
圣湘生物 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法) |
泰熙生物 | 新型冠狀病毒IgM/IgG檢測試劑盒 |
萬孚生物 | 2019-nCoV新型冠狀病毒抗體檢測試劑(免疫層析法) |
2019-nCoV新型冠狀病毒IgM抗體檢測試劑(熒光免疫層析法) | |
2019-nCoV新型冠狀病毒抗體檢測試劑(熒光免疫層析法) | |
新產業生物 | 全自動化學發光新型冠狀病毒2019-nCoVIgM、IgG抗體檢測試劑盒 |
亞輝龍 | 化學發光法新冠病毒抗體檢測試劑盒 |
一瑞生物 | 新型冠狀病毒COVID-19抗體檢測試劑盒(膠體金法) |
之江生物 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法) |
卓誠惠生 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法) |
碩世生物 | 新型冠狀病毒(2019)核酸檢測試劑盒(熒光PCR法) |
新型冠狀病毒IgM/IgG抗體聯合檢測試劑盒(膠體金法) | |
安圖生物 | 新型冠狀病毒(2019-nCoV)IgG抗體檢測試劑盒(磁微粒化學發光法) |
新型冠狀病毒(2019-nCoV)IgM抗體檢測試劑盒(磁微粒化學發光法) | |
新型冠狀病毒(2019-nCoV)IgM/IgG雙抗體檢測試劑盒(膠體金法) | |
新型冠狀病毒2019-nCoV核酸檢測試劑盒(PCR-熒光探針法) | |
科華生物 | 新型冠狀病毒(2019-nCoV)ORF1ab/N/E基因核酸檢測試劑測試劑盒(熒光PCR法) |
新型冠狀病毒(SARS-CoV-2)IgM/IgG抗體檢測試劑盒(膠體金法) | |
新型冠狀病毒(SARS-CoV-2)IgM抗體檢測試劑盒(ELISA法) | |
新型冠狀病毒(SARS-CoV-2)IgG抗體檢測試劑盒(ELISA法) | |
凱創生物 | 新型冠狀病毒(2019-nCoV)IgM/IgG總抗體快速檢測試劑盒(膠體金法) |
新型冠狀病毒(2019-nCoV)IgM抗體快速檢測試劑盒(膠體金法) | |
中元匯吉 | 新型冠狀病毒(2019-nCoV)核酸檢測試劑盒(PCR-熒光探針法) |
核酸提取試劑盒(磁珠法) | |
銀科醫學 | 新型冠狀病毒IgG/IgM抗體檢測試劑盒(膠體金法) |
明德生物 | 新型冠狀病毒(2019-nCoV)核酸檢測試劑盒 |
新型冠狀病毒IgM/IgG抗體檢測試劑盒(膠體金法) | |
康華生物 | 新型冠狀病毒IgM抗體檢測試劑盒(免疫層析法) |
基蛋生物 | 新型冠狀病毒(2019-nCOV)核酸檢測試劑盒(熒光PCR法) |
新型冠狀病毒(2019-nCOV)IgM抗體檢測試劑盒(膠體金法) | |
新型冠狀病毒(2019-nCOV)IgG抗體檢測試劑盒(膠體金法) | |
新型冠狀病毒(2019-nCOV)IgM/IgG抗體檢測試劑盒(膠體金法) | |
國賽生物 | 新型冠狀病毒IgG/IgM抗體檢測試劑盒(時間分辨熒光免疫法) |
諾唯贊 | 新型冠狀病毒(2019-nCoV)IgM/IgG抗體檢測試劑盒(膠體金法) |
微米生物 | 新型冠狀病毒(COVID-19)IgM/lgG抗體檢測試劑 |
博奧賽斯 | 新型冠狀病毒(COVID-19)抗體檢測試劑盒(膠體金免疫層析法) |
新型冠狀病毒(COVID-19)IgG抗體檢測試劑盒(膠體金免疫層析法) | |
新型冠狀病毒(COVID-19)IgM抗體檢測試劑盒(膠體金免疫層析法) | |
新型冠狀病毒(COVID-19)IgG抗體檢測試劑盒(化學發光法法) | |
新型冠狀病毒(COVID-19)IgM抗體檢測試劑盒(化學發光法法) | |
新型冠狀病毒(COVID-19)IgG抗體檢測試劑盒(酶聯免疫法) | |
新型冠狀病毒(COVID-19)IgM抗體檢測試劑盒(酶聯免疫法) | |
美聯泰科生物 | 新型冠狀病毒IgG抗體檢測試劑盒(磁微粒化學發光法) |
新型冠狀病毒IgM抗體檢測試劑盒(磁微粒化學發光法) | |
新型冠狀病毒S1蛋白檢測試劑盒(磁微粒化學發光法) | |
伊仕生物 | 新冠狀病毒(2019-NCOV)IgG/IgM抗體聯合檢測試劑盒(膠體金法) |
寶太生物 | 新型冠狀病毒IgG/IgM抗體檢測試劑盒(膠體金法) |
萬泰生物 | 新型冠狀病毒(2019-nCoV)抗體檢測試劑盒(膠體金法) |
新型冠狀病毒(2019-nCoV)抗體檢測試劑盒(酶聯免疫法) | |
新型冠狀病毒(2019-nCoV)IgM抗體檢測試劑盒(酶聯免疫法) | |
新型冠狀病毒(2019-nCoV)核酸檢測試劑盒(PCR-熒光探針法) | |
英盛生物 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法) |
康錄 | 新型冠狀病毒(COVID-19)核酸檢測試劑盒(熒光PCR法) |
三諾生物 | 新型冠狀病毒抗體檢測試劑盒(膠體金法) |
艾克韋 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法) |
安必奇生物 | 新型冠狀病毒(COVID-19)IgM/IgG抗體檢測試劑盒(膠體金免疫層析法) |
比格飛序生物 | 新型冠狀病毒核酸擴增檢測試劑盒 |
波生生物 | 新型冠狀病毒IgM/IgG抗體檢測試劑盒(膠體金法) |
博日科技 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法) |
丹娜生物 | 新型冠狀病毒(2019-nCoV)IgG抗體檢測試劑盒(膠體金法) |
新型冠狀病毒(2019-nCoV)核酸檢測試劑盒(RT-PCR多重熒光探針法) | |
達伯藥業 | 新型冠狀病毒(SASA-CoV-2)IgG抗體診斷試劑盒(膠體金法) |
新型冠狀病毒(SASA-CoV-2)IgM抗體診斷試劑盒(膠體金法) | |
新型冠狀病毒(SASA-CoV-2)IgG/IgM抗體診斷試劑盒(膠體金法) | |
新型冠狀病毒(SASA-CoV-2)核酸檢測試劑盒(熒光RT-PCR法) | |
迪安生物 | 新型冠狀病毒核酸檢測試劑盒(熒光PCR法) |
禾柏生物 | 新型冠狀病毒IgG/IgM抗體檢測試劑盒(膠體金法、免疫比濁法) |
華益美生物 | 新型冠狀病毒(2019-nCoV)核酸檢測試劑盒(PCR-熒光法) |
簡碼基因 | 新型冠狀病毒核酸檢測試劑盒(快速PCR熒光法) |
萊和生物 | 新型冠狀病毒(2019-nCoV)IgG抗體檢測試劑(膠體金法) |
新型冠狀病毒(2019-nCoV)IgM抗體檢測試劑(膠體金法) | |
新型冠狀病毒(2019-nCoV)IgM/lgG抗體聯合檢測試劑(膠體金法) | |
樂普醫療 | 新型冠狀病毒抗體檢測試劑盒(膠體金免疫層析法) |
黎明生物 | 新型冠狀病毒(SARS-COV-2)多重RT-PCR試劑盒(熒光探針法) |
新型冠狀病毒IgM及IgG抗體二聯檢測試劑盒(乳膠免疫層析層析法) | |
新型冠狀病毒總抗體檢測試劑盒(乳膠免疫層析層析法) | |
新型冠狀病毒抗原檢測試劑盒(乳膠免疫層析層析法) | |
隆基生物 | 新型冠狀病毒檢測試劑盒(COIVD-19) |
默樂生物 | 新型冠狀病毒(2019-nCoV)ORF1ab、E和N基因檢測試劑盒(熒光PCR法) |
新型冠狀病毒IgG/IgM抗體檢測試劑盒(免疫層析法) | |
納奧生物 | 新型冠狀病毒(COVID-19)多重核酸快速PCR檢測試劑盒 |
普瑞康 | 新型冠狀病毒試劑盒 |
深藍醫療 | 新型冠狀病毒(COVID-19)IgM/IgG抗體檢測試劑盒(膠體金免疫層析法) |
新型冠狀病毒(COVID-19)IgM抗體檢測試劑盒(膠體金免疫層析法) | |
新型冠狀病毒(COVID-19)lgG抗體檢測試劑盒(膠體金免疫層析法) | |
思路迪 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(光PCR法) |
新型冠狀病毒2019-nCoV和流感AB核酸聯合檢測試劑盒(四色光PCR法) | |
泰格科信 | 新型冠狀病毒(2019-nCoV)IgG/IgM抗體檢測試劑盒(膠體金法) |
天深醫療 | 新型冠狀病毒IgM抗體檢測試劑盒(化學發光法) |
新型冠狀病毒IgG抗體檢測試劑盒(化學發光法) | |
新產業 | 全自動化學發光新型冠狀病毒2019-nCoVIgM、IgG抗體檢測試劑盒 |
新健康成 | 新型冠狀病毒(SARS-Cov-2)IgG/M檢測試劑盒(免疫熒光層析法) |
英科新創 | 新型冠狀病毒IgM/IgG抗體聯合檢測試劑盒(膠體金法) |
新型冠狀病毒IgM/IgG抗體聯合檢測試劑盒(膠體金法)-帶配件 | |
新型冠狀病毒抗體檢測試劑盒(膠體金法) | |
新型冠狀病毒抗體檢測試劑盒(膠體金法)-帶配件 | |
致善生物 | 新型冠狀病毒SARS-CoV-2核酸檢測試劑盒(熒光PCR法) |
喜諾生物 | 新型冠狀病毒IgG抗體檢測試劑盒(膠體金法) |
新型冠狀病毒IgM抗體檢測試劑盒(膠體金法) | |
嵐煜生物 | 新型冠狀病毒(2019-nCoV)IgM/IgG檢測試劑盒 |
揚新生物 | (SARS-CoV-2)IgM抗體檢測試劑盒(膠體金法) |
(SARS-Cov-2)IgM/IgG抗體檢測試劑盒(膠體金法) | |
(SARS-CoV-2)IgM抗體檢測試劑盒(熒光法) | |
(SARS-CoV-2)IgM/IgG抗體檢測試劑盒(熒光法) | |
2019-nCoV核酸檢測試劑盒 | |
良潤生物 | 新型冠狀病毒IgM/IgG抗體檢測試劑盒(膠體金免疫層析法) |
華銀醫藥 | 新型冠狀病毒2019-nCOV核酸檢測試劑盒(熒光PCR法) |
麗拓生物 | 新型冠狀病毒(COVID-19)IgG/IgM檢測試劑盒(免疫層析法) |
泰樂德醫療 | 新型冠狀病毒(SARS-CoV-2)核酸檢測試劑盒(PCR-熒光探針法) |
新型冠狀病毒(SARS-CoV-2)IgM/IgG抗體檢測試劑盒(膠體金法) | |
新型冠狀病毒(2019-nCoV)核酸檢測試劑盒(雙重熒光PCR法) | |
宇諾生物 | 新型冠狀病毒(SARS-CoV-2)IgG/IgM抗體聯合檢測試劑盒(膠體金法) |
億立方 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(PCR-熒光探針法) |
新型冠狀病毒COVID-19IgG、IgM抗體檢測試劑盒(膠體金法) | |
新賽亞 | 新型冠狀病毒(2019-nCoV)IgM抗體檢測試劑盒(膠體金免疫層析法) |
新型冠狀病毒(2019-nCoV)lgG抗體檢測試劑盒(膠體金免疫層析法) | |
新型冠狀病毒(2019-nCoV)lgM抗體檢測試劑盒(量子點免疫熒光法) | |
新型冠狀病毒(2019-nCoV)lgG抗體檢測試劑盒(量子點免疫熒光法) | |
沃文特生物 | 2019-nCoVIgG/IgM抗體檢測試劑盒 |
優利特 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法) |
金磁納米 | 新型冠狀病毒(2019-nCoV)核酸檢測試劑盒 |
(2019-nCoV)IgG/IgM抗體檢測試劑盒 | |
康永生物 | 新型冠狀病毒抗體IgG/IgM聯合檢測試劑盒(膠體金法) |
北京庫爾科技 | 新冠病毒(2019-nCoV)IgM/IgG抗體檢測試劑盒(膠體金層析法) |
寶瑞源生物 | 新型冠狀病毒(SAR-CoV-2)核酸檢測試劑盒(多重熒光PCR法) |
安科生物 | 新型冠狀病毒(COVID-19)IgG/IgM抗體檢測試劑盒(膠體金法) |
東方基因 | 新型冠狀病毒(COVID-19)IgG/IgM抗體快速檢測試紙(全血/血清/血漿) |
新型冠狀病毒SARS-COV-2核酸檢測試劑盒(熒光PCR法) | |
杭州優思達 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(恒溫擴增-實時熒光法) |
海爾施基因科技 | SARS-CoV-2VirusDetectionDiagnosticKit(RT-qPCRMethod) |
方欣生物 | 新型冠狀病毒(COVID-2019)抗體檢測試劑盒 |
新型冠狀病毒(COVID-2019)IgG抗體檢測試劑盒 | |
新型冠狀病毒(COVID-2019)IgM抗體檢測試劑盒 | |
中檢安泰 | 新型冠狀病毒(COVID-19)IgA/IgM/IgG抗體聯合檢測試劑會(膠體金法) |
融智生物 | 七項呼吸道病毒核酸聯檢試劑盒(微流控RT-PCR法) |
英諾特生物 | 新型冠狀病毒IgM/lgG抗體膠體金檢測試劑 |
申瑞生物 | 新型冠狀病毒2019-nCoV及流感病毒核酸檢測試劑盒(熒光PCR法) |
麗珠試劑 | 新型冠狀病毒(2019-nCoV)IgM/IgG抗體檢測試劑盒(膠體金法) |
芯超生物 | 新型冠狀病毒(2019-nCoV)抗體檢測試劑盒(膠體金法) |
光景生物 | 新型冠狀病毒(SARS-CoV-2)IgG/IgM抗體檢測試劑盒(時間分辨熒光免疫層析法) |
中生捷諾 | 新型冠狀病毒(2019-nCoV)核酸檢測試劑盒(熒光PCR法) |
德諾生物 | 新型冠狀病毒(2019-nCoV)IgG抗體檢測試劑盒(膠體金免疫層析法) |
新型冠狀病毒(2019-nCoV)IgM抗體檢測試劑盒(膠體金免疫層析法) | |
新型冠狀病毒(2019-nCoV)抗原檢測試劑盒(熒光免疫層析法) | |
威斯騰生物 | 新型冠狀病毒(COVID-19)核酸檢測試劑盒(PCR熒光探針法) |
萬類生物 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法) |
拜澳泰克 | 2019新型冠狀病毒核酸檢測試劑盒(熒光RT-PCR法) |
2019新型冠狀病毒核酸檢測試劑盒(恒溫顯色法) | |
博奧生物 | 六項呼吸道病毒核酸檢測芯片試劑盒(恒溫擴增芯片法) |
迅敏康 | 新型冠狀病毒(2019-nCoV)核酸檢測試劑盒(PCR-熒光探針法) |
檢康生物 | 冠狀病毒IgM和IgG雙抗體快速檢測試劑盒 |
金匙醫學 | 新型冠狀病毒核酸檢測試劑盒(多重熒光RT-PCR法) |
博暉創新 | 新型冠狀病毒IgM/IgG抗體檢測試劑盒 |
新型冠狀病毒2019-nCoV核酸檢測試劑盒 | |
微遠基因 | 宏基因組(mNGS)新型冠狀病毒核酸檢測試劑盒 |
陽普醫療 | 新型冠狀病毒(SARS-CoV-2)核酸檢測試劑盒(PCR-熒光探針法) |
迪瑞醫療 | 新型冠狀病毒IgM抗體檢測試劑盒(化學發光免疫分析法) |
新型冠狀病毒IgG抗體檢測試劑盒(化學發光免疫分析法) | |
優尼德生物 | SARS-CoV-2核殼蛋白(IgG抗體+IgM抗體+總抗體)ELISA試劑盒 |
數據來源:公開資料整理
相比歐盟CE認證而言,美國市場的準入門檻更高。截止2020年4月27日,核酸檢測產品已獲得美國EUA的40余家企業中,多為業內知名的跨國巨頭企業,其中有四家中國企業:華大基因、南京科維思、邁克生物、復星醫藥;而核酸檢測產品已同時取得國內NMPA注冊證書、歐盟CE認證和美國FDAEUA的國內企業只有華大基因、邁克生物、復星醫藥三家公司。
獲得FDAEUA認證的國內核酸檢測產品
獲得FDAEUA認證的國內核酸檢測產品 | ||
獲批企業 | 獲批時間 | 產品 |
華大基因 | 2020年3月27日 | 新型冠狀病毒SARS-nCoV-2核酸檢測試劑盒(熒光PCR法) |
南京科維思 | 2020年4月6日 | 新冠病毒(COVID-19)檢測試劑盒(數字PCR法) |
邁克生物 | 2020年4月15日 | 新冠病毒核酸檢測試劑盒(熒光PCR法) |
復星醫藥 | 2020年4月17日 | 新型冠狀病毒2019-nCov核酸檢測試劑盒(熒光PCR法) |
數據來源:公開資料整理
在
抗體檢測產品中,樂普醫療的新型冠狀病毒(SARS-CoV-2)抗體檢測試劑盒(膠體金免疫層析法)于3月27日取得FDAEUA準入,安圖生物的新型冠狀病毒抗體檢測試劑盒(膠體金法,英文名稱:Anti-SARS-CoV-2RapidTest)于2020年4月24日獲得FDAEUA認證。此外,國內企業萬孚生物、三諾生物等的抗體檢測試劑盒也已按照FDA發布的《PolicyforDiagnosticTestsforCoronavirusDisease-2019duringthePublicHealthEmergency》完成Notification程序,并且完成了公司注冊和產品列名,標志著公司該產品具備了在美國上市銷售的資格。2020年4月25日,我國商務部發布公告,“自4月26日起,取得國外標準認證或注冊的新型冠狀病毒檢測試劑、醫用口罩、醫用防護服、呼吸機、紅外體溫計的出口企業,報關時須提交書面聲明,承諾產品符合進口國(地區)質量標準和安全要求,海關憑商務部提供的取得國外標準認證或注冊的生產企業清單驗放”。這也就意味著新冠檢測產品的出口只需要取得國外標準認證或注冊,無需擁有國內注冊證。但同時很重要的一點是出口企業必須進入中國醫藥保健品進出口商會企業清單才能被驗放。目前,符合規定的企業都在積極申請加入,截至4月28日,已有51家企業進入清單。而在此前2020年3月31日,國家商務部會同海關總署、國家藥監局發布《關于有序開展醫療物資出口的公告》(2020年第5號),要求自4月1日起,同時獲得NMPA注冊證書和國外特定區域準入資格的企業可實現國內及獲授權的國外地區新冠檢測產品的銷售。此次“雙證”限制的放開,進一步促進國內IVD企業的新冠檢測產品出口。
4、國內外新冠檢測試劑盒需求測算
1)國內新冠檢測試劑盒需求測算
截至2020年3月底,國內新冠檢測數量(含核酸及抗體檢測)在1500萬人份以上,包含確診患者、高危人群以及疑似病例的排除等,其中國內確診患者從確診到出院全流程至少需要檢測5次。核酸檢測收費國內基本上在150元-270元(各地區及檢測機構有所差異,主要分為醫院和第三方檢測機構,第三方檢測機構價格高于醫院),抗體檢測收費在100元左右,絕大多數醫保承擔,部分自費隔離患者自己承擔。
4月24日,湖北省在全國范圍內率先開始新冠病毒檢測試劑集中采購。4月26日,湖北省藥械集中采購服務平臺發布《湖北省新型冠狀病毒相關檢測試劑集中采購擬中選企業公示》,本次湖北新冠病毒檢測試劑集采共有19家企業申報競價,其中14家申報核酸檢測試劑組,5家申報抗體檢測試劑組。結果共有4家企業中標核酸檢測試劑盒(邁克生物、達安基因、武漢明德生物、華大生物),2家企業中標檢測試劑盒(珠海麗珠、南京諾唯贊),采購執行周期原則上為1年。我們以中標公司報價的平均值作為檢測試劑的平均出廠價,計算得出核酸檢測產品平均出廠價為21.417元,抗體檢測產品平均出廠價13.393元。我們預計后續其他省份也將陸續開展集采工作,新冠檢測收費價格也將對應下降。
湖北省新型冠狀病毒相關檢測試劑集中采購擬中選企業名單及報價
湖北省新型冠狀病毒相關檢測試劑集中采購擬中選企業名單及報價 | ||
類別 | 注冊人名稱 | 報價價格(元) |
核酸檢測試劑 | 邁克生物股份有限公司 | 16780 |
中山大學達安基因股份有限公司 | 19998 | |
武漢明德生物科技股份有限公司 | 23900 | |
華大生物科技(武漢)有限公司 | 24990 | |
抗體檢測試劑 | 珠海麗珠試劑股份有限公司 | 12900 |
南京諾唯贊醫療科技有限公司 | 13885 | |
數據來源:公開資料整理
對于2020年國內新冠檢測的需求測算,我們分為以下四個假設:1)醫院現存確診患者以及住院、陪護等檢測:根據國家發布的《新冠肺炎診療方案第七版》中的相關規定,保守估計現存確診患者每人治愈出院前進行兩次核酸檢測,共需2280次檢測。我們還要關注醫院住院病人以及陪護人員的情況,全國多地都出臺了對住院患者及陪護人員進行新冠肺炎檢測的政策,例如黑龍江省政府規定4月16日起二級及以上醫療機構對所有入院患者和陪護人員開展核酸和血清抗體檢測,浙江大學醫學院附屬第二醫院對3000多位住院病人開展新型冠狀病毒核酸檢測和新型冠狀病毒血清抗體檢測,做到應檢盡檢。對這部分人群的測算,首先根據2016-2018年每年醫院入院人數保守估計2020年將達到20216萬人次,假設一個患者有一名人員陪同,他們都將進行一次檢測,推測得到檢測需求量為40432萬次。與此同時,假設每位醫護人員進行2次檢測,那么推算共需要2400萬次。
2)境外輸入檢測:當前國內疫情防控積極向好的態勢來之不易,對于境外輸入環節的防控堅決不能放松。北京、上海等多個入境點城市都發布了對所有入境人員全面落實集中醫學觀察和核酸檢測的規定。根據北京市疾控中心介紹,4月1日至4月13日期間,入境人員累計3122人,據此我們保守估計一個月全國入境人員為2萬人。由于全球疫情原因,各個國家對出入境都進行了嚴格把關,入境人員短期內并不會出現大的增幅。按照2020年剩下8個月計算,假設今年累計入境16萬人次,每人進行一次核酸檢測,故需要16萬次檢測。
3)復工、復學檢測:許多企業都會組織復工復產的員工進行核酸檢測,進一步確保安全性。截至4月14日,全國規模以上工業企業平均開工率已達99%,其它行業也基本復工,還未復工的僅為少數。我們假設還有100萬的跨省市復工人員,每人進行一次檢測,推算檢測需求量為100萬次。同時,教師群體以及學生群體也是重點目標人群,不少省市地區在近日宣布將會在開學之后對返校師生進行“核酸檢測”,廣州已經對20.8萬名首批復學的高三、初三師生員工,全覆蓋開展核酸檢測。根據教育部披露的2018年在校師生的數據,以此為基礎進行測算。假設每位師生進行一次核酸檢測,預計檢測需求量也將達到2.93億次。
4)常態化檢測:當前疫情防控已經進入常態化。4月22日,中共中央政治局常委、國務院總理、中央應對新冠肺炎疫情工作領導小組組長李克強主持召開領導小組會議,會議指出做好常態化防控要提升檢測能力,大規模開展核酸和抗體檢測。日前,上海率先發布了單位或個人可自愿自費預約進行核酸檢測的通知,截至4月24日,已經有北京、上海、廣州、山西、天津等地公布了新冠檢測機構。我們對于自愿檢測的人群數量進行了預估,假設東部發達地區的檢測比率是5%,中西部地區的檢測比率是3%,推算自愿檢測需求達到5390萬次。綜上,根據我們的推算,國內從目前到今年年底檢測需求量共計為77641.42萬次,我們假設其中70%為核酸檢測,30%為抗體檢測。以湖北省中標公司報價的平均值作為出廠價,最終推算得到國內新冠檢測的市場規模約為147.59億元。
國內從目前到2020年年底新冠檢測新增需求測算
國內從目前到2020年年底新冠檢測新增需求測算 | |||||
住院患者及醫護人員檢測 | |||||
- | 人數(萬) | 人均檢測次數(次) | 檢測需求量(萬) | ||
全國現有確診人數 | 0.114 | 2 | 0.2 | ||
預計2020年醫院入院情況 | 20216 | 1 | 20216 | ||
入院患者陪護情況 | 20216 | 1 | 20216 | ||
醫護人員 | 1200 | 2 | 2400 | ||
境外輸入檢測 | |||||
- | 人數(萬) | 人均檢測次數(次) | 檢測需求量(萬) | ||
預計全國每月入境(萬) | 總人數(萬) | ||||
入境情況 | 2 | 16 | 1 | 16 | |
復工、復學檢測 | |||||
- | 人數(萬) | 人均檢測次數(次) | 檢測需求量(萬) | ||
復工人群省際流動 | 100 | 1 | 100 | ||
教師 | 1700 | 1 | 1700 | ||
學生 | 27600 | 1 | 27600 | ||
自愿檢測 | |||||
- | 人數(萬) | 人均檢測次數(次) | 檢測需求量(萬) | ||
總人數(萬) | 假設檢測比例 | 檢測人數(萬) | |||
東部發達地區 | 56538.51 | 5% | 2826.93 | 1 | 2826.93 |
中西部地區 | 85443.28 | 3% | 2563.3 | 1 | 2563.3 |
國內檢測市場測算 | |||||
- | 核酸檢測 | 抗體檢測 | 總體 | ||
檢測需求(萬次) | 54346.9 | 23291.53 | 77638.42 | ||
檢測市場(億元) | 116.4 | 31.19 | 147.59 | ||
數據來源:公開資料整理
2)國外新冠檢測試劑盒需求測算
2020年3月以來,國外疫情爆發,先是在歐美等發達國家迅速傳播,近期第三世界國家如南美、非洲等地疫情日漸嚴重,同時暴露出新冠檢測試劑盒供應不足的問題,我們選擇一些典型的發達國家以及發展中國家對于未來幾個月全球(除中國)新冠試劑盒的需求進行測算。根據現有各國新型冠狀病毒確診情況以及檢測情況的數據,我們選取了目前確診人數大于5000的國家,推算了整個疫情期間各國的檢測試劑需求量。首先計算出“現已檢測總次數/總確診數”,對疫情發展做出“情景1”、“情景2”、“情景3”三種假設情況下的預測。在情景1下,我們假設發達國家未來新增患者數是現在確診人數的2倍,發展中國家未來新增患者數是現在確診人數的4倍;情景2按照發達國家3倍、發展中國家5倍;情景3按照發達國家4倍、發展中國家6倍進行假設,以此為基礎推算出未來預計需要檢測的次數。同時,對于未來疫情好轉之后的常態化檢測也進行預估,假設發達國家總人口的檢測比率為5%,發展中國家相對低一些為3%。
由于發展中國家醫療服務能力較低,醫療物資非常匱乏,通常檢測標準較低。假設:1)發達國家確診患者治愈出院需要經過兩次檢測,而在發展中國家只需進行一次檢測。2)發達國家核酸試劑盒平均出廠價32.2元,抗體試劑盒平均出廠價20.1元(按照比國內價格高50%計算)。所有檢測試劑盒中70%為核酸試劑盒,30%為抗體試劑盒。3)發展中國家的試劑盒平均出廠價要低于發達國家,假設核酸試劑盒平均出廠價27.9元,抗體試劑盒平均出廠價17.5元(按照比國內價格高30%計算)。使用的所有檢測試劑盒中30%為核酸試劑盒,70%為抗體試劑盒。
最終預測得到,在情景1假設下,全球(除中國)新增市場規模將合計超過10.78億美元;在情景2假設下,全球(除中國)新增市場規模將合計超過11.84億美元;在情景3假設下,全球(除中國)新增市場規模將合計超過12.90億美元。表11以情景2為例,測算疫情發展期間現存患者、預計新增患者需要檢測的次數,以及疫情達到平穩狀態后常態化檢測的需求:
疫情期間國外新型冠狀病毒試劑盒市場規模測算(不含常態化檢測)
疫情期間國外新型冠狀病毒試劑盒市場規模測算(不含常態化檢測) | |||||
疫情發展情況 | 發達國家 | 發展中國家 | 全球市場(億美元) | ||
預計新增患者數/現總確診數 | 檢測試劑市場(億美元) | 預計新增患者數/現總確診數 | 檢測試劑市場(億美元) | ||
情景1 | 2 | 1.73 | 4 | 1.05 | 2.78 |
情景2 | 3 | 2.54 | 5 | 1.3 | 3.84 |
情景3 | 4 | 3.34 | 6 | 1.56 | 4.91 |
數據來源:公開資料整理
國外新型冠狀病毒試劑盒市場規模測算(情景2、含常態化檢測)
國外新型冠狀病毒試劑盒市場規模測算(情景2、含常態化檢測) | |||||
發達國家 | 發展中國家 | ||||
- | 檢測次數(次) | 市場規模(元) | - | 檢測次數(次) | 市場規模(元) |
核酸檢測 | 80,459,107 | 2,590,783,258 | 核酸檢測 | 74,229,391 | 2,070,999,998 |
抗體檢測 | 34,482,475 | 693,097,739 | 抗體檢測 | 173,201,911 | 3,031,033,450 |
總體 | 114,941,582 | 3,283,880,998 | 總體 | 247,431,302 | 5,102,033,447 |
假設檢測中核酸檢測占比70%,抗體檢測占比30%假設核酸檢測出廠價32.2元,抗體檢測出廠價20.1元(按照比國內價格高50%計算) | 假設檢測中核酸檢測占比30%,抗體檢測占比70%假設核酸檢測出廠價27.9元,抗體檢測出廠價17.5元(按照比國內價格高30%計算) | ||||
國外檢測試劑市場規模>83.86億人民幣(11.84億美元) | |||||
數據來源:公開資料整理

 公眾號
公眾號
 小程序
小程序
 微信咨詢
微信咨詢


















![2026年中國餐飲行業產業鏈圖譜、營收規模、競爭格局、上市企業對比及未來競爭趨勢分析:百勝中國營收規模遙遙領先[圖]](http://img.chyxx.com/images/2022/0330/dd2a6e2dd1963d26c8672c625ba6166e69bd4120.png?x-oss-process=style/w320)
![2026年中國人用疫苗行業政策、產業鏈、批發情況、競爭格局及發展趨勢分析(附上市企業疫苗經營現狀、區域分布):綜合性龍頭將在市場中占據絕對主導[圖]](http://img.chyxx.com/images/2022/0330/b388a599ab8b82a70e79838a8b0d600efa11727f.png?x-oss-process=style/w320)
![研判2026!中國海纜行業分類、市場規模、重點企業及中標項目分析:深遠海開發倒逼輸電技術跨越式升級,國產±500kV直流海纜實現百公里級突破[圖]](http://img.chyxx.com/images/2022/0330/ce25a2275c336b52d58303ed80fb7924b3fd1022.png?x-oss-process=style/w320)
![2026年中國電子數據取證行業發展歷程、政策、發展現狀、競爭格局及趨勢研判:網絡犯罪高發推動需求增長,電子數據取證市場規模達34.17億元[圖]](http://img.chyxx.com/images/2022/0408/1ba88a0bac4b4a65439b806124f6fc0f4ab03cad.png?x-oss-process=style/w320)
![研判2026!中國健康險AI科技行業進入壁壘、產業鏈、市場規模、競爭格局及未來發展趨勢分析:CR10市場占有率達58.5%[圖]](http://img.chyxx.com/images/2022/0330/d1363a7ee3953fc25ed09e0b79158acce9dc7c22.png?x-oss-process=style/w320)
