一、2020年中國醫療器械行業的政策動向
醫療器械是指直接或者間接用于人體的儀器、設備、器具、體外診斷試劑及校準物、材料以及其他類似或者相關的物品,包括所需要的計算機軟件。一般來說,醫療器械可以分為高值醫用耗材、低值醫用耗材、醫療設備、IVD(體外診斷)四大類。其中根據使用用途不同,又可以將高值醫用耗材市場分為骨科植入、血管介入、神經外科、眼科、口腔科、血液凈化、非血管介入、電生理與起搏器、其他共九小類。
“十一五”以來,國家對醫療器械的發展越來越重視,“十二五”國家將把醫療器械納入戰略發展內,“十三五”醫療器械已經到了蓄勢待發,大發展的趨勢。
十三五期間我國醫療器械產業將重點發展五個領域,包括數字化診療設備、組織修復與可再生材料、分子診斷儀器及試劑、人工器官與生命支持設備,健康監測裝備這五大方面。此外,還會圍繞養老健康、殘障等方面進行布局。
這五個重點發展領域中,數字化診療設備將做“十三五”重點專項的首發。“十三五”期間國家對醫療器械和醫療裝備有很高的支持,醫療器械產業有拉動內需,改善民生的重要功能,同時它能夠帶動多學科交叉融合,帶動科技創新和制造水平發展,是我國國民經濟轉型和結構調整的戰略指導點。
在高端醫療影像產業化方面,顯然主流的高端影像設備,高質量、高分辨率、以及多種功能,以及新的影像設備,仍然是十三五重點關注的部分。診療一體化是重要趨勢,在影像引導下的規劃也是十三五重點發展的領域,特別是高端影像相結合。可再生組織修復的材料和可吸收植介入材料也是非常重要的趨勢。
智能醫療有助于解決醫療資源分布不均的難題,但開發出具有醫療信息監測,健康信息監測、評估、調控的終端或者是軟件系統或者是硬件終端是目前醫療器械行業的一個當務之急,大量的健康信息智能檢測微型化需要整個行業來發力。
隨著疫情的發展,中國醫療器械行業將被推到浪潮的最前沿,急需口罩,防護服,呼吸器和工具包等醫療設備。在政策方面,國家衛生與健康委員會和國家食品藥品監督管理局相繼發布了醫療器械政策;在防疫投資方面,許多企業參與了物質捐贈。
新型冠狀病毒最初于1月7日由專家診斷。國內體外診斷企業迅速投入了試劑的研發,國家藥品監督管理局(SFA)同步采取行動,啟動了緊急審批程序。批準的總期限從123個工作日減少到13個工作日;體外診斷試劑可用于減少臨床試驗病例數或免除臨床試驗,并且在產品上市后繼續進行注冊時將提交臨床應用數據摘要報告。
1月,國家食品藥品監督管理局發布了關于緊急進口未在中國注冊的醫療器械的意見,為進口醫療器械開了綠燈。為了滿足流行病的需要,可以緊急地從國外進口符合美國,歐盟和日本相關標準的醫療器械。如果企業能夠提供海外醫療器械清單認證文件和檢驗報告,并做出產品質量和安全承諾,則可以在緊急情況下使用。
根據緊急批準程序,國家食品藥品監督管理局在1月26日,28日和31日分別批準了4種產品,2種產品和1種產品。1月26日,試劑盒由華大生物學,枝江生物學和杰諾生物學生產;1月28日,該試劑盒由Daan基因生產。1月31日,該試劑盒由盛祥生物和博捷醫療生產。
海關總署發布公告,充分保證對進口藥品,消毒用品,防護用品,醫療器械等的預防控制物料以快速通過海關。應當在通關現場設置專門的驗收窗口和快速清除進口捐贈物資的綠色通道,以實現快速檢查和放行。對于用于防疫的,具有國家進口藥品管理許可證的醫療材料,海關可以先經藥品主管部門的證明予以放行,然后辦理有關手續。
智研咨詢發布的《2020-2026年中國醫療器械及硬件行業市場專項調查及投資盈利分析報告》顯示:2019年12月A股共有3家企業成功上市;12月起5家醫療器械公司新提交上市申請;至少3家醫療器械公司排隊上市;10家左右醫療器械公司在上市輔導。醫療器械行業企業上市情況反映了醫療器械行業的發展勢頭迅猛。
2019年12月-2020年1月中國醫療器械上市公司口碑
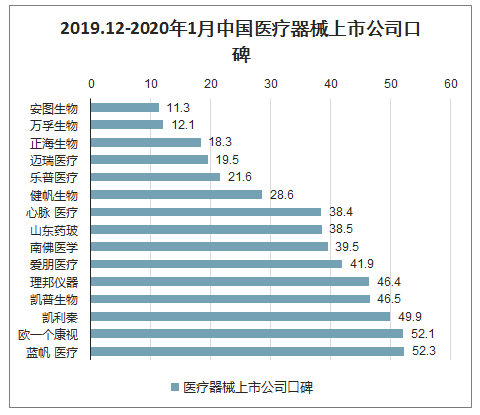
數據來源:公開資料整理
二、海外疫情升溫,全球對中國制造醫療物資設備依賴度高
目前已多家國內醫療器械領域企業接到大量海外訂單,進一步彌補了一季度醫療器械公司非疫情相關產品業績損失。目前國內新冠疫情得到有效控制,各行業都在有序復工復產,而隨著海外疫情蔓延升溫,全球對中國的醫療物資設備產品依賴度進一步提高。由于疫情嚴重國家確診人數暴增,醫療系統已逼近超載,海外市場對醫療物資例如口罩、額溫槍、防護服、呼吸機、監護儀等產品需求激增,使相關產品量價齊升。
魚躍醫療抗疫相關產品訂單增長迅猛。呼吸機從疫情之前的日產300臺,已經提升至日產700臺以上,目前海外訂單在五千臺左右,增長勢頭比較快。額溫槍需求大增,目前魚躍醫療日產量達到了3.2萬支,現在已經為海外市場提供了超過50萬只的額溫槍。魚躍醫療制氧機、電子血壓計、康復產品中均有通過美國食藥監局(FDA)認證款型。此外西班牙對外銀行向魚躍醫療采購2000臺呼吸機、400臺制氧機。
邁瑞醫療收到了大量海外訂單,包括亞太地區、歐洲和中東,其中意大利的訂單中包含8000臺監護和1500臺呼吸機。試劑盒方面,華大基因的檢測試劑盒國際訂貨量已超過60萬人份,覆蓋50余個國家和地區,并已陸續運抵日本、文萊、泰國、阿聯酋、埃及、秘魯等地。
疫情期間醫療器械上市公司產品出海情況
產品 | 上市公司 | 詳細 |
試劑盒 | 迪瑞醫療 | 2項醫療器械產品于近日取得了CE認證證書 |
試劑盒 | 迪安診斷 | 新型冠狀病毒檢測產品獲得英國MHRA注冊的公告 |
ProtectiveMask(防護口罩)和MedicalMask(醫用口罩) | 翰宇藥業 | 公司全資子公司口罩產品獲得歐盟CE認證 |
試劑盒 | 安科生物 | 全資子公司新型冠狀病毒檢測產品獲得歐盟CE認證 |
試劑盒 | 安科生物 | 關于新型冠狀病毒檢測產品獲得歐盟CE認證 |
試劑盒 | 科華生物 | 新型冠狀病毒檢測相關產品取得歐盟自由銷售證書 |
試劑盒 | 華大基因 | 新型冠狀病毒核酸檢測試劑盒產品已啟動美國食品藥品監督管理局(FDA)的EUA申報,目前Pre-EUA已被正式受理 |
皮膚黏膜消毒系列產品 | 康恩貝公司 | 獲得了消毒劑產品的歐盟CE認證 |
試劑盒 | 康恩貝 | 康恩貝參股的浙江檢康生物技術公司的新型冠狀病毒快速檢測試劑盒成功獲得歐盟CE認證 |
防護口罩 | 巨星科技 | 公司的防護口罩已在歐盟完成了醫療器械備案注冊 |
試劑盒 | 新邦制藥 | 全資子公司產品獲得歐盟準入資格 |
一次性使用醫用口罩 | 三鑫醫療 | 一次性使用醫用口罩通過CE符合性 |
防護口罩 | 巨星科技 | 產品獲得美國FDA批準 |
試劑盒 | 樂普醫療 | 新型冠狀病毒抗體檢測試劑盒(膠體金免疫層析法)取得歐盟CE認證 |
試劑盒 | 三諾生物 | 新型冠狀病毒檢測產品獲得歐盟準入資格 |
試劑盒 | 碩世生物 | 新型冠狀病毒(2019)核酸檢測試劑盒(熒光PCR法)獲得歐盟CE認證 |
試劑盒 | 萬孚生物 | 三款新型冠狀病毒檢測產品取得了歐盟頒發的CE認證 |
試劑盒 | 邁克生物 | 公司新型冠狀病毒核酸檢測試劑盒已獲得歐盟CE認證 |
試劑盒 | 凱普生物 | 新型冠狀病毒2019-nCoV核酸檢測試劑盒(熒光PCR法)獲得歐盟CE認證 |
試劑盒 | 達安基因 | 公司新型冠狀病毒核酸檢測試劑盒已獲得歐盟CE認證 |
試劑盒 | 美康生物 | 新型冠狀病毒COVID-19抗體(IgM/IgG)聯合檢測試劑盒(乳膠法)3月2日獲得歐盟準入資格 |
試劑盒 | 華大基因 | 全資子公司產品取得歐盟自由銷售證書 |
試劑盒 | 美康生物 | 新型冠狀病毒COVID-19核酸檢測試劑盒(熒光PCR法)已獲得歐盟準入資格 |
試劑盒 | 復星醫藥 | 控股子公司上海復星長征醫學科學有限公司有若干新型冠狀病毒檢測試劑盒已通過歐盟CE認證 |
呼吸機、額溫槍、制氧機、電子血壓計、康復產品 | 魚躍醫療 | 抗疫產品呼吸機的訂單增長勢頭比較快;額溫槍疫情爆發后產品需求大增;公司制氧機、電子血壓計、康復產品中均有通過美國食藥監局(FDA)認證款型;西班牙對外銀行向魚躍醫療采購2000臺呼吸機、400臺制氧機。 |
監護儀、呼吸機 | 邁瑞醫療 | 公司收到了許多海外訂單,包括亞太地區、歐洲和中東,其中意大利最為緊急。訂單中包含8000臺監護和1500臺呼吸機。 |
監護儀 | 寶萊特 | 收到意大利訂單超過1000臺高端監護儀 |
血氣產品、病人監護、心電診斷、超聲影像等 | 理邦儀器 | 意大利血氣產品訂單達20余臺。公司產品遠銷全球170多個國家和地區,涉及公司全部業務產線,即病人監護、心電診斷、超聲影像等。 |
數據來源:公開資料整理
三、醫療器械領域“新基建”:加強醫院科室建設、分級診療、加速進口替代以及發展檢驗實驗室
疫情期間,中央多次會議強調從體制機制上健全國家公共衛生應急管理體系,創新和完善重大疫情防控舉措,提高應對突發重大公共衛生事件的能力水平,表明在疫情穩定過后,國家一定會加大力度推進公共衛生制度改革。在國家逐步完善公共衛生體系的背景下,未來在政策層面上的改革將會很大程度上影響醫療器械領域。
加強醫院科室建設、推動分級診療將有利于醫療器械市場進一步實現放量;疫情暴露的醫療器械國產化率低、自主應急保障能力不足的問題加大了國家扶持國產的決心,利好國產醫療器械企業搶占市場份額;疫情過后醫療衛生領域的數字化建設也將重塑醫療器械行業格局,醫療器械企業加速完成數字化轉型迫在眉睫。
1、醫院科室建設、分級診療促使醫療器械市場擴容
疫情期間的經驗教訓將是加強醫院科室建設成為疫情過后的重要任務,推動分級診療政策、促進各級醫院科室設備配置升級、醫院加大采購將促使醫療器械市場擴容。疫情期間由于醫院患者數量暴增,暴露了我國醫院重癥科室數量少、醫療設備仍然非常欠缺、難以滿足臨床需要的問題,重癥科室建設迫在眉睫。目前,我國醫療市場ICU僅占普通病房約6%,遠遠低于發達國家的15%,國內醫療資源發達地區的ICU服務病床數為醫院病床總數的不到2%,醫生/護士人數與床位數比例分別低于0.8:1和2.5:1,均不滿足衛生部發布的《中國重癥加強治療病房(ICU)建設和管理指南》規定的標準。
醫療市場ICU占普通病房比重
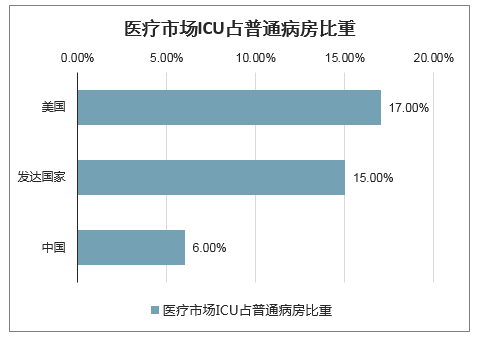
數據來源:公開資料整理
疫情過后,隨著國家大力推進各級醫院重癥科室的建設,并逐步升級科室相關醫療設備配置,未來利好監護儀、呼吸機、輸注泵、除顫儀、超聲儀器等相關科室急需配備的產品以及相關生產廠商。此次疫情期間,核酸檢測試劑盒在對新冠病毒的檢測和篩查中發揮了至關重要的作用,未來國家對流感檢測試劑的需求有望進一步加大,利好試劑生產企業,檢測更高效更準確的試劑產品將占有更大市場。同時,國家將更加重視分級診療政策的推進和實施,促進醫療資源的下沉,醫療器械基層市場有望進一步擴容。
ICU配備醫療器械以及相關生產廠商
分類 | ICU | 配備醫療器械相關生產廠商 |
診斷 | DR | 上海聯影、深圳安科、邁瑞醫療、萬東醫療 |
CT | 機 | 上海聯影、深圳安科、邁瑞醫療、萬東醫療 |
血球儀 | 邁瑞醫療、理邦儀器核酸提取儀 | 科華生物 |
熒光 | PCR儀 | 科華生物 |
監護 | 監護儀 | 邁瑞醫療 |
血氧儀 | 邁瑞醫療、理邦儀器、魚躍醫療 | |
血氣分析儀 | 邁瑞醫療、理邦儀器 | |
血液分析 | 開立醫療 | |
治療 | 呼吸機 | 邁瑞醫療、魚躍醫療 |
制氧機 | 邁瑞醫療、魚躍醫療 | |
除顫儀 | 邁瑞醫療、魚躍醫療 | |
輸注泵 | 邁瑞醫療 | |
檢測 | 檢測試劑盒 | 華大基因、碩世生物、達安基因、西隴科學、科華生物、萬孚生物等 |
治療耗材 | 血濾耗材 | 健帆生物、寶萊特 |
數據來源:公開資料整理
2、加速進口替代,推動國產設備高端化,打開國產醫療器械在高端市場的增長空間。
疫情穩定后推進進口替代的政策將加速實施,將推動國產設備高端化,有利于打開國產醫療器械在高端市場的增長空間。此次疫情暴露出我國醫療設備國產化率仍然比較低的問題,新冠病毒肺炎應用的重要治療和診斷設備核心技術和品牌主要掌握在外資企業手中,并且國產醫療器械以中低端產品為主,在中高端市場占有率仍然偏低,以檢測試劑細分領域為例,高端檢測試劑的上游核心原材料主要由羅氏等外資龍頭企業所壟斷。國產的中高端CT機、超聲設備、檢驗儀器、磁共振設備以及心電圖機的市場占有率均低于30%。
部分高端醫療器械國產及進口比重對比
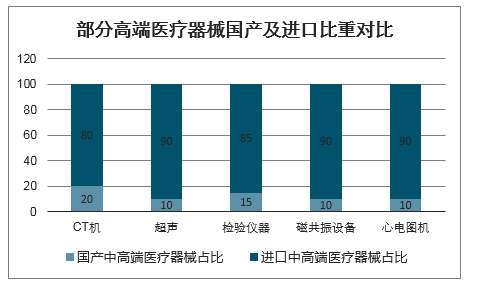
數據來源:公開資料整理
近平主席在北京考察新冠肺炎防控科研攻關工作時指出“要加快補齊我國高端醫療裝備短板,加快關鍵核心技術攻關,突破技術裝備瓶頸,實現高端醫療裝備自主且可控。疫情過后,隨著國家加大對醫療衛生領域的投入,鼓勵國產醫療器械企業加強科技創新,未來在醫療設備高端領域有望看到更多國產核心技術和品牌的出現。
3、檢驗實驗室增長空間廣闊
新冠疫情中無論在中國還是在海外,檢驗實驗室都在疫情的檢測、預防、控制等方面發揮了重要的作用。此次疫情湖北省先后分五批擴充核酸檢測機構的數量,包括66家醫療機構、18家疾控中心和13家第三方機構,共有97家檢測機構開展核酸檢驗檢測。檢驗實驗室已經成為預防、檢測疾病的不可或缺的社會力量。以武漢金域為例,疫情期間,武漢金域停止了其他所有檢測業務,只進行新冠病毒的檢測,以武漢金域實驗室相關團隊為基礎,在當地又派出了114名相關專業人員,日均檢測量達3000例左右,1月30日湖北全省檢測能力單日4000例。此次美國新冠疫情檢測數量已經達到全世界最多,而絕大部分檢測是由檢驗實驗室完成。
美國檢驗實驗室和CDC檢測樣本數量
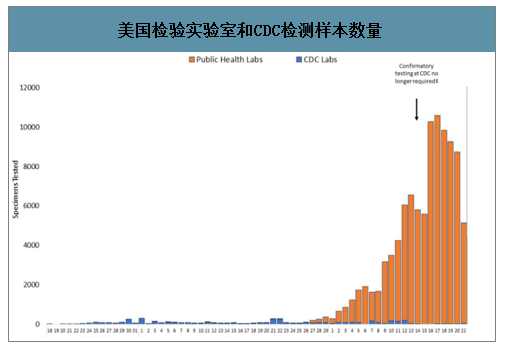
數據來源:公開資料整理
截至2018年末,我國共有獨立醫學檢驗實驗室1495家,比2017年同比增長73.4%。目前我國第三方醫學檢驗市場規模在140億元左右,占整個醫學檢驗市場份額的比例不足5%,未來增長空間大。相關標的:短期看,推薦海外疫情嚴重國家所急需如呼吸機、試劑盒等產品相關公司,長期推薦ICU重癥科室建設所需產品相關公司、第三方檢驗實驗室,建議關注:邁瑞醫療、魚躍醫療、萬孚生物、金域醫學、迪安診斷。
醫療器械相關標的情況(2020年3月31日)
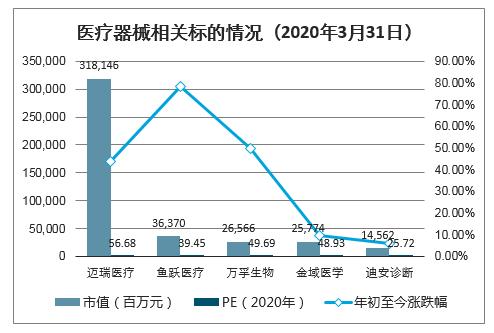
數據來源:公開資料整理
四、我國醫療器械行業市場前景
隨著全球居民生活水平的提高和醫療保健意識的增強,近年來,醫療器械產品需求持續增長。數據顯示,截至2018年底,我國醫療器械行業市場規模達到了5304億元,預計2022年我國醫療器械行業市場規模將超9000億元,其行業市場前景十分廣闊。
2017-2022年中國醫療器械行業市場規模及增長走勢
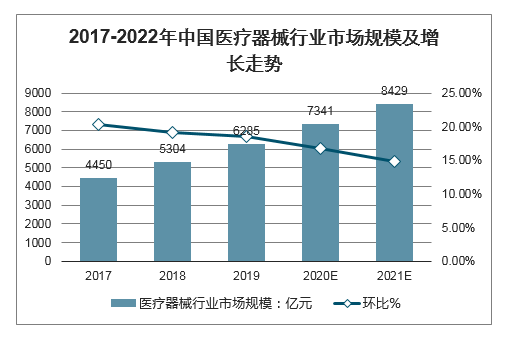
數據來源:公開資料整理
 智研咨詢 - 精品報告
智研咨詢 - 精品報告

2026-2032年中國運動再生醫學醫療器械行業市場研究分析及投資前景研判報告
《2026-2032年中國運動再生醫學醫療器械行業市場研究分析及投資前景研判報告》共八章,包含國內運動再生醫學醫療器械生產廠商競爭力分析, 2026-2032年中國運動再生醫學醫療器械行業發展前景及投資策略, 運動再生醫學醫療器械企業投資戰略與客戶策略分析等內容。

 公眾號
公眾號
 小程序
小程序
 微信咨詢
微信咨詢























