政府對藥械創新產業大力支持,國務院和國家食藥監總局相繼發出《關于改革藥品醫療器械審評審批制度的意見》、《關于鼓勵藥品醫療器械創新改革臨床試驗管理的相關政策》、《關于鼓勵藥品醫療器械創新實施藥品醫療器械全生命周期管理的相關政策》和《關于鼓勵藥品醫療器械創新加快新藥醫療器械上市審評審批的相關政策》等一系列文件以及支持性的政策,使創新藥械審批進一步加快,國內藥械企業和研究機構創新積極性不斷提高,我國進入藥械創新發展的“加速期”。
鼓勵、推動創新的重磅政策
|
政策
|
時間
|
內容
|
優勢
|
|
關于改革藥品醫療器械審批制度的意見
|
2015.8
|
提高上市藥品審批標準,推進仿制藥一致性評價,鼓勵創新(制度、審評創新)
|
鼓勵研究和創制新藥,提升新藥研發效率
|
|
關于解決藥品注冊申請積壓實行優先審評審批的意見
|
2016.2
|
對創新藥和臨床急需藥品進行優先審評
|
優先審評制度減少了新藥排隊時間、提高研發效率、加快新藥上市
|
|
化學藥品注冊分類改革
|
2016.3
|
新 5 類:根據風險程度分為創新藥和仿制藥,根據原創性分為創新藥和改良型新藥
|
嚴格定義創新藥:結構明確的新化學實體
|
|
藥品上市許可持有人MAH
|
2016.6
|
生產權和上市權分離(批件持有人和生產企業分離)
|
解放創新:輕資產研發型企業有望脫穎而出,CMO、CRO、CSO 專業分工迎來發展機遇
|
|
關于深化審評審批制度改革鼓勵藥品醫療器械創新的意見
|
2017.10
|
加快臨床急需藥品和醫療器械的上市審評速度、解決公眾用藥需求、鼓勵創新等 6 大方面
|
提高我國醫藥產業的創新發展水平,激發醫藥研發的活力,解決臨床急需藥品和醫療器械短缺難題
|
|
接受藥 品境外 臨床試驗數據的
|
2018.7
|
對接受境外臨床試驗數據的適用范圍、基本原則、完整性要求、數據提交的技術要求以及接受程度均給予明確
|
鼓勵創新藥企業進行全球多中心的臨床試驗
|
|
中華人民共 和國藥品管理法
|
2019.8
|
鼓勵具有新的治療機理,治療嚴重危及生命的疾病、罕見病的新藥和兒童用藥的研制;對臨床急需的短缺藥、防治重大傳染病和罕見病等疾病的新藥、兒童用藥開設綠色通道,優先審評審批。
|
強調藥品的治療價值,鼓勵研發創新,加速創新藥上市流程
|
數據來源:公開資料整理
一、醫保改革
2019 年 8 月,醫保局發布《國家基本醫療保險、工傷保險和生育保險藥品目錄》,是我國繼 2000 年、2004 年、2009 年、2017 年后的第五版醫保目錄。常規準入品種方面,2019 版目錄包括西藥 1322 個、中成藥 1321 個,總數較 2017 版目錄差別不大,但調出、調入的品種數量較多,其中新增的 148 個品種覆蓋了要優先考慮的國家基本藥物、癌癥及罕見病等重大疾病治療用藥、慢性病用藥、兒童用藥等,藥品結構進一步改善。
談判準入品種方面,2017 年和 2018 年,醫保目錄通過談判方式分別納入了 36 個和17 個藥品,此次調整初步確定 128 個藥品納入擬談判準入范圍,治療領域主要涉及癌癥、罕見病等重大疾病、丙肝、乙肝以及高血壓、糖尿病等慢性病等。對于 2017年談判準入的、協議將于 2019 年底到期且目前尚無仿制藥上市的 31 個藥品的續約談判也將同步進行。
從全世界范圍而言,醫保藥品目錄動態調整機制早已被世界上多數國家采用,美國、法國的新藥從上市到進入報銷目錄的時間是 6 個月左右,日本是 3 個月,德國、英國僅為 1 個月。在世界發達國家和地區,醫療市場競爭高度激烈又受到嚴格監管,醫保藥品目錄是各方極為重要的保障醫療質量和控費的手段,而動態調整機制是國際上大多數國家采用的做法,有諸多成功的經驗可以借鑒。目前我國醫保目錄調整頻率逐步加快,創新藥進入醫保時間縮短,有望快速實現放量。
2018 年下半年,由國家醫保局牽頭針對 32 個仿制藥品種進行了 11 個城市的帶量采購,除 6 個產品流標以外,剩余產品以平均 52%的降幅中標,仿制藥利潤空間被大幅壓縮,醫藥板塊也因帶量采購出現大幅回調。到 2019 年四月中旬,25 個中選品種在 11 個試點地區采購總量達到了 4.38 億片,總金額達 5.33 億,完成約定采購總量的 27.31%,采購進度遠遠超出市場預期。
在我國,醫保是醫療服務最大的支付方,2008 年后,由于醫保支出增速持續高于醫保收入增速,使得醫保結余率不斷降低,醫保進入控費階段。2017 年,醫保收入增速有所回升,醫保控費初見成效,醫保結余率有所上升,后續醫保政策從整體控費調整為結構調整,創新藥及器械的競爭優勢明顯。
2003-2018年醫保收支增速基本匹配
數據來源:公開資料整理
醫保結余率穩步回升
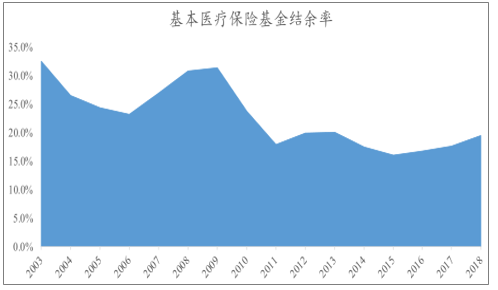
數據來源:公開資料整理
二、創新藥
我國目前創新藥迎來了最良好的環境,研發時機逐步走向成熟,我國從市場、人才、科研條件、研究基礎等各方面都為創新藥物的研發提供了廣闊的“沃土”。從資金面來看,國家對創新藥研發的財政支持不斷加大,資本市場對創新藥的追逐愈加激烈,融資金額與案例數不斷增多,為創新藥研發奠定基礎。
2016-2020年國家重大新藥創制專項經費投入(億元)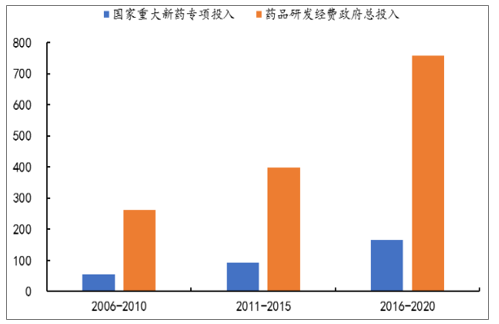
數據來源:公開資料整理
人才層面,國家采用多渠道引進國際人才,構建高端人才體系,促進原創新藥研發產業發展。
在國家政策的大力扶持下,國內生物醫藥園區建設迅猛發展,經國家有關部門或地方政府批準的生物醫藥園區已有 50 多個。隨著我國生物產業園區的產業化支撐環境不斷優化,新藥研發產業鏈正逐步向生物醫藥產業園區聚集和延伸,創新型生物醫藥園區正在成為我國創新藥物產業化實施的主體。
隨著我國創新藥研發環境的不斷改善,我國創新藥企業的研發能力逐漸得到世界認可。越來越多的企業利用“授權許可( license-out)”方式布局海外創新藥市場,通過轉讓產品的海外權益,在避免建立海外銷售渠道高昂成本的同時獲得較為可觀的現金流,反哺公司在國內的研發活動,形成良性循環。
從需求面來講,人口老齡化、城鎮化和醫保的全面鋪開將成為消費量方面的強大驅動力,經濟增長、人們對健康的迫切需求將成為消費升級方面的強大驅動力,強大的需求也為我國創新藥的發展奠定堅實基礎。與美國發達的商業醫療保險不同,我國商業醫療保險發展程度較低,在基本醫療保險之外,居民醫療費用基本由個人承擔,目前隨著居民可支配收入的增加,人民對健康重視程度的加大,人均醫療保健支出也在快速增長,成為拉動醫藥行業長期發展的巨大動力。
我國居民人均醫療保健支出快速增長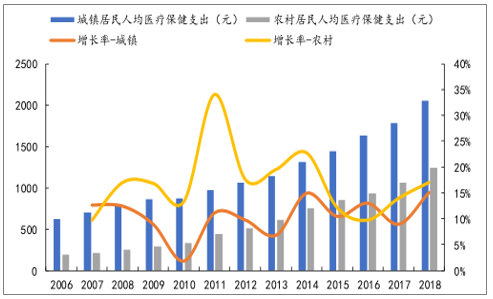
數據來源:公開資料整理
之前由于消費能力較低,高價藥品在我國市場較小,隨著我國人居收入的逐步增加,規模逐漸壯大的富裕人群對醫療提出新需求,不僅對高端的醫療服務需求增大,更提高了對高端藥品的消費需求,從我國已經上市的創新藥銷售情況來看,阿帕替尼、康柏西普等高價藥品在未進醫保之前銷售額也實現了快速增長,足以證明我國居民在高端醫療方面的支出潛力十分巨大。目前出境醫療成為新的熱點,除了國外醫療服務環境更好之外,一個重要的原因是很多國外已經上市的高端藥品在我國并沒有被批準上市,所以只有到國外才有機會使用部分高端藥品,也從側面反映出目前國內市場對高價值創新藥的需求強勁,但供給相對不足,創新藥有望在需求的強勁拉動下快速發展。
隨著近幾年國內生物類似藥研發、生產能力的提升,以及監管政策的逐步推進與完善,我國生物制品行業迎來蓬勃發展,其中抗體類藥物發展尤為迅猛。
國內生物類似藥監管政策匯總
|
時間
|
政策
|
評價
|
|
2007
|
《藥品注冊管理辦法》
|
生物制品按照新藥申請的程序申報
|
|
2015
|
《生物類似藥研發與評價技術指導原則(試行)》
|
對生物類似藥的定義和研發都給出了明確的指導意見
|
|
2016
|
《藥品注冊管理辦法》(修訂版)
|
進一步規范生物類似藥的概念,對生物類似藥的研發和申報做了規定
|
|
2017
|
《生物制品通用名命名原則規程》(征求意見稿)
|
生物類似藥的命名規范,規范生物制品通用名方法
|
數據來源:公開資料整理
2014-2018 年我國生物藥市場規模從 1167 億元增至 2622億元,復合增長率 22.4%,增速遠高于全球水平,預計 2023 年將增長至超過 6000億,而其中抗體藥物增速最快,從 2014 年的 74 億增長至 2018 年的 160 億,預計2023 年有望達到 1500 億的市場規模。
2014-2023年中國生物制品市場規模及預測( 億元 )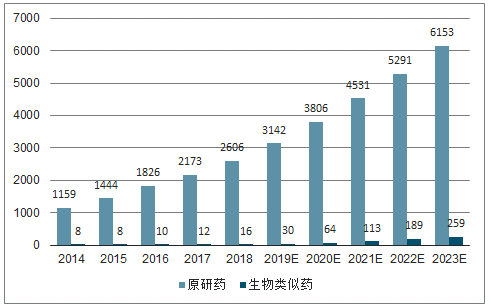
數據來源:公開資料整理
2014-2023年中國抗體藥物市場規模趨勢及預測(億元)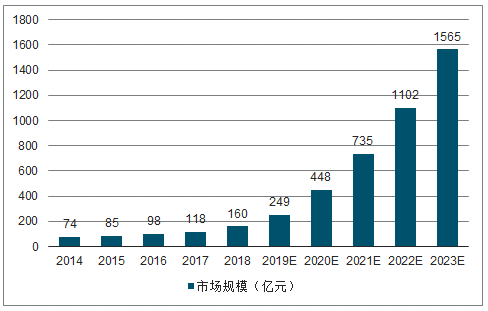
數據來源:公開資料整理
隨后我國企業君實、信達和恒瑞的 PD-1 也相繼實現上市,百濟神州的 PD-1 也有希望于 2019年上市,后續仍有復宏漢霖、中山康方和嘉和生物等多家企業處于臨床三期、二期狀態。
國內其他 PD-1研發管線
|
進度
|
公司 名稱
|
通用名
|
適應癥
|
|
NDA
|
百濟神州
|
特雷利珠單抗
|
霍奇金淋巴瘤
|
|
III 期
|
復宏漢霖
|
HLX10
|
非小細胞肺癌
|
|
小細胞肺癌
|
|||
|
食管癌
|
|||
|
中山康方
|
AK105
|
非小細胞肺癌
|
|
|
賽諾菲
|
Cemiplimab
|
晚期非小細胞肺癌
|
|
|
II 期
|
嘉和生物
|
GB226
|
B 細胞非霍奇金淋巴瘤
|
|
譽衡藥業
|
GLS-010
|
霍奇金淋巴瘤
|
|
|
泰州翰中
|
HX008
|
MSI-H/實體瘤
|
|
|
百奧泰
|
BAT1306
|
EBV相關性胃癌
|
|
|
I 期
|
麗珠單抗
|
LZM009
|
晚期實體瘤
|
|
新時代藥業
|
F520
|
晚期實體瘤
|
|
|
神州細胞
|
重組人源 PD-1 單抗
|
晚期實體瘤
|
|
|
石藥集團
|
SG001
|
惡性腫瘤
|
|
|
邁博太科
|
CMAB819
|
肝細胞癌、非小細胞肺癌
|
|
|
安科生物
|
SSI-361
|
晚期實體瘤
|
|
|
瑞陽制藥
|
RB-004
|
惡性腫瘤
|
|
|
思坦維
|
STW204
|
實體瘤
|
數據來源:公開資料整理
目前國產 PD-1 產品中,恒瑞的卡瑞利珠在新適應癥拓展和藥物聯用方面進展較快。目前已獲批經典霍奇金淋巴瘤,后續肝癌二線、食管癌二線以及非小細胞肺癌一線治療方案已經提交上市申請并納入優先審批,進度較為領先。同時,恒瑞充分發揮抗癌藥物產品線豐富的特點,開展了卡瑞利珠與靶向藥阿帕替尼、廣譜抗癌藥紫杉醇以及多個化療藥物的聯合治療方案,未來有望帶動整個抗腫瘤產品線。
我國 PD-1 市場空間預計超過 500 億。目前 PD-1 已經在黑色素瘤、霍奇金淋巴瘤、非小細胞肺癌、肝癌和結直腸癌等癌種上表現出了顯著的治療效果,參照目前 O 藥和 K 藥在 FDA 獲批的適應癥以及相關指南的使用指導,結合我國各種癌種的發病人數可初步計算出我國 PD-1 的市場空間約為 500 億,其中食管癌、肝癌、結直腸癌和非小細胞肺癌等領域市場規模較大,預計未來隨著 PD-1 適應癥的逐步拓展,市場空間有望進一步加大。
相比于化學仿制藥,受到研發難度較大、藥政法規不健全等問題,我國生物類似藥研發起步較晚,進入 21 世紀初才逐步由企業進入單抗領域,隨后在研發能力增強以及藥審政策改革的推進下,近幾年很多企業布局生物類似藥,生物類似藥研發進入繁榮期,前期布局的企業經過 10 年的研發儲備,已經率先進入收獲期,2019 年復星醫藥旗下復宏漢霖的利妥昔單抗生物類似藥率先上市,百奧泰的國內首個阿達木單抗生物類似藥格樂立(BAT1406)獲批上市,以及曲妥珠單抗類似藥等也已經紛紛進入申報上市階段,生物類似藥將引領我國制藥企業的新一輪成長。
2014-2030年中國生物類似藥市場規模級預測 (億元)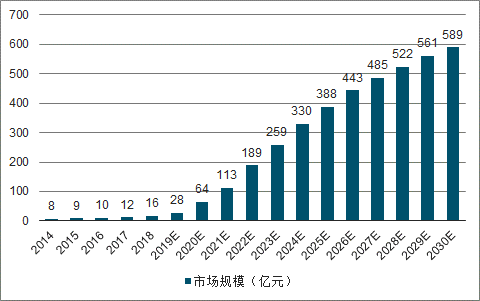
數據來源:公開資料整理
三、國內 CRO
隨著基礎試驗費用增長和監管要求日益嚴格,臨床前研究的時間增長,臨床試驗規模更大,臨床試驗的失敗率不斷增加,新藥開發成本出現迅速增長,給制藥企業的研發帶來巨大壓力。
2010-2018年新藥研發投資回報率趨勢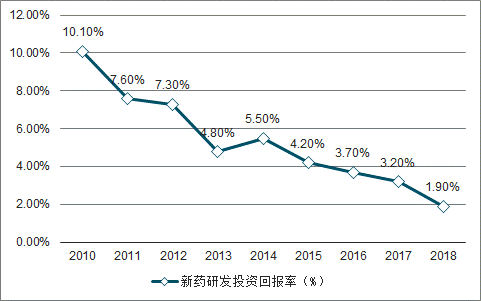
數據來源:公開資料整理
面對不斷增加的研發成本,越來越多的國外制藥企業開始尋求海外布局,進軍中國市場,自建 CRO 企業的同時,把研發業務外包給中國本土的 CRO 企業,中國相比于國外,在人才、成本上都有著巨大的優勢,隨著國外產能向國內的轉移,國內誕生了以藥明康德、康龍化成為代表的一批大型 CRO 公司,其業務主要集中在臨床前研發階段,且大部分收入均來自于海外業務。
2017-2018年本土 CRO企業海外業務收入 (億元)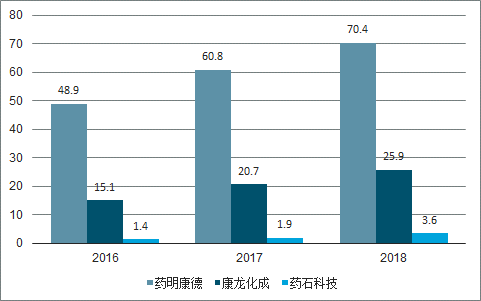
數據來源:公開資料整理
國產 1 類新藥申請受理數量明顯增加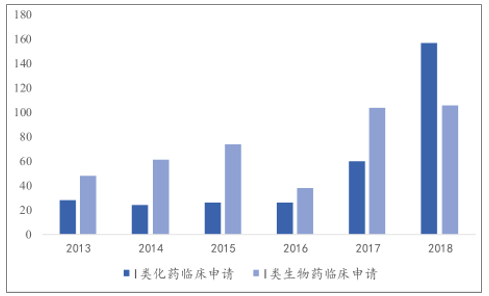
數據來源:公開資料整理
在目前醫保支付結構調整、帶量采購等大的政策背景下,轉型創新勢在必行,研發投入均快速增加,恒瑞醫藥、信立泰、華東醫藥和科倫藥業等企業研發營收占比均達到 10%,逐步向國際制藥巨頭看齊,本土制藥企業的轉型為 CRO 帶來強大的成長動力。
我國龍頭醫藥企業研發投入占比向海外企業看齊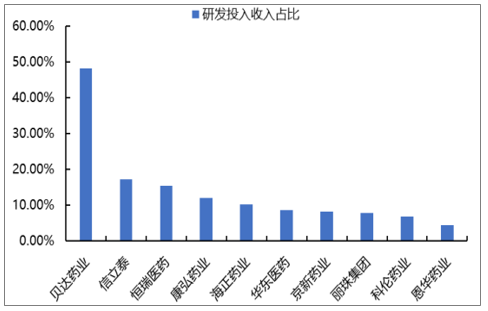
數據來源:公開資料整理
隨著國家鼓勵創新以及藥品審評審批的改革,我國初創型創新藥企業如雨后春筍般壯大,風險資本對于醫藥研發領域的關注度也越來越高,新藥研發成為最活躍的投資領域之一。從 2014 年開始,我國醫藥研發領域融資額快速增加,進入 2018 年更是有大幅提升,遠高于全球增速。對于研發型初創企業,絕大部分融資均用于創新藥的研發,由于初創企業研發實力較弱,不能單獨完成創新藥研發的全部環節,所以必然選擇 CRO 企業進行部分研發外包,從而進一步打開 CRO 市場空間。
2010-2018年我國業醫藥企業 VC/PE 融資額快速增加
數據來源:公開資料整理
我國登記的臨床試驗數量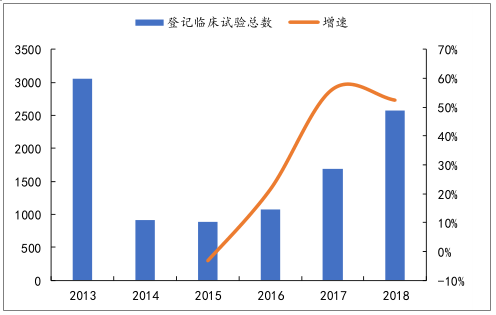
數據來源:公開資料整理
伴隨著創新藥研發的火熱,國內臨床試驗開設數量也在大幅增加,根據藥物臨床試驗登記與信息公示平臺統計數據,從 2014 年開始,每年登記的臨床數量均維持大幅增加,2018 年登記的臨床數量達到 2570 個,其中國際多中心臨床試驗占比達到8.06%,也在逐年提升,快速增加的臨床數量最直觀的反應了 CRO 行業的快速成長。
2019 年 3 月,CDE 發布《化學仿制藥參比制劑目錄(第二十一批)》,首次發布 242個注射劑參比制劑。同年 10 月,NMPA 公開征求《化學藥品注射劑仿制藥質量和療效一致性評價技術要求(征求意見稿)》《已上市化學藥品注射劑仿制藥質量和療效一致性評價申報資料要求(征求意見稿)》意見,就注射劑一致性評價的技術要求和申報資料等進行了進一步的完善,國內注射液一致性評價有望提速。目前,CDE受理注射液一致性評價申請四百余個,涉及一百多個品種。
2015-2018年仿制藥一致性評價BE 登記數量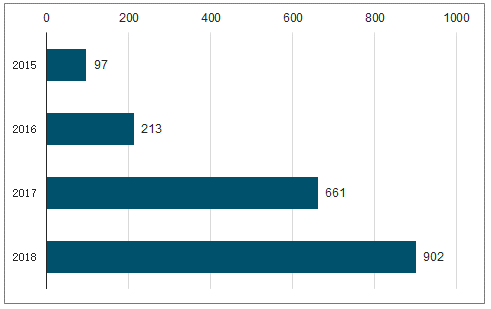
數據來源:公開資料整理
一致性評價的執行力度大、時間緊、范圍廣,從整個仿制藥一致性評價的流程來看,從準備一致性評價方案到全部完成申報至少需要兩年的時間,企業要保證重要品種及時完成一致性評價,必然要將大部分工作外包給 CRO 機構,具有品牌知名度的龍頭 CRO 企業必將受益。
相關報告:智研咨詢發布的《2019-2025年中國創新藥行業市場運行態勢及投資方向研究報告》

 公眾號
公眾號
 小程序
小程序
 微信咨詢
微信咨詢


















![2026年中國合成生物行業發展全景分析:下游應用從醫藥健康、化工材料向農業食品、能源環保全面滲透,行業已展現出巨大的應用潛力[圖]](http://img.chyxx.com/images/2022/0408/55d853aceb464ffcf6fad7c27bbd7795797b1b5a.png?x-oss-process=style/w320)
![2026年中國骨密度儀行業產業鏈圖譜、采購總量、采購金額、獲批企業、競爭格局及未來競爭趨勢分析:外資品牌占據主導地位[圖]](http://img.chyxx.com/images/2022/0330/e060dd24be7392f76ddd0a84489963879d953ac6.png?x-oss-process=style/w320)
![研判2026!中國物聯網行業概念、市場規模、企業競爭格局分析:中國物聯網產業領跑全球,AI融合驅動“泛在智聯”新紀元[圖]](http://img.chyxx.com/images/2022/0330/ce25a2275c336b52d58303ed80fb7924b3fd1022.png?x-oss-process=style/w320)
![研判2026!中國汽車行業分類、產銷量、重點企業銷量分析:一季度中國汽車行業現“內冷外熱”分化,出口同比激增成核心增量引擎[圖]](http://img.chyxx.com/images/2022/0330/ff5315f651f3e124d0f5a156ac51655e46e5433f.png?x-oss-process=style/w320)
![2026年中國彩鋼板行業發展歷程、供需情況、市場規模、競爭格局及趨勢研判:彩鋼板市場規模達1138.76億元,鋼結構與綠色建材政策驅動增長[圖]](http://img.chyxx.com/images/2022/0330/4279f04d08c7260a105d321a303d34a91af3a3d5.png?x-oss-process=style/w320)
![2026年中國UV燈管行業產業鏈、發展現狀、競爭格局、競爭趨勢分析:外資壟斷高端賽道,中低端市場競爭白熱化[圖]](http://img.chyxx.com/images/2022/0330/b388a599ab8b82a70e79838a8b0d600efa11727f.png?x-oss-process=style/w320)
