一、1 1-10月累計批簽發量同比小幅下滑2%,環比降幅縮窄,免疫規劃疫苗份額提升
行業概況:2019年1-10月,疫苗行業整體批簽發量為44630萬支,同比下滑2%,下滑幅度較1-9月明顯縮窄,主要受長生生物疫苗事件及疫苗法出臺監管趨嚴導致批簽發速度下降影響,現階段批簽發速度已有提升。 2011-2018年,行業整體批簽發量由79402.9萬支下降到54076.3萬支,CAGR為-4.7%;
品類結構:行業整體批簽發量前三大類分別是肝炎、 腦膜炎及百白破系列,合計市場份額為44%。 1-10月:肝炎類疫苗批簽發量同比下滑16%,市場份額小幅下降至16%。 腦膜炎類疫苗批簽發量同比下滑6%,市場份額下降至12%。 百白破系列疫苗批簽發量同比增長15%,市場份額穩定在15%;
疫苗類型:國家免疫規劃品種市場份額由2011年的30%提高到2019年10月底的50%,非國家免疫規劃品種市場份額由2011年的70%降低到2019年10月底的50%。 短期來看,隨著非國家免疫規劃的重磅產品獲批上市,有望擴大非國家免疫規劃品種整體市場份額。 長期來看,隨著行業的發展及國家衛生戰略的調整,未來國家免疫規劃品種有可能再度擴容;
疫苗行業全品種2011年以來批簽發量統計
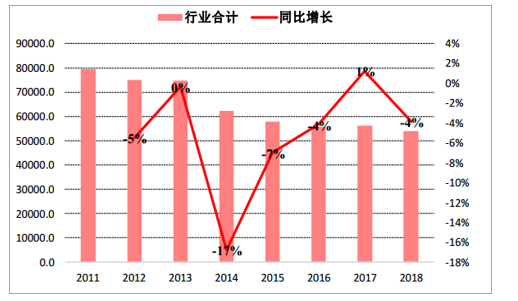
數據來源:公開資料整理
疫苗行業全品種近年1-10月累計批簽發量
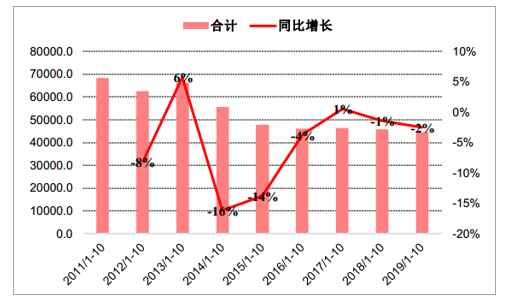
數據來源:公開資料整理
近年疫苗品種競爭格局
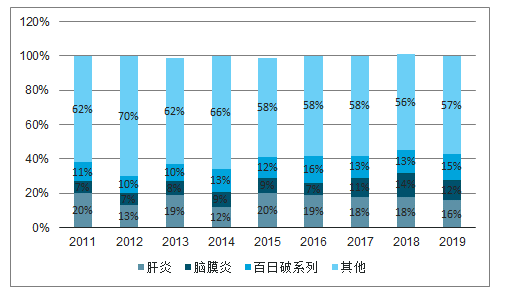
數據來源:公開資料整理
近年疫苗種類市場格局
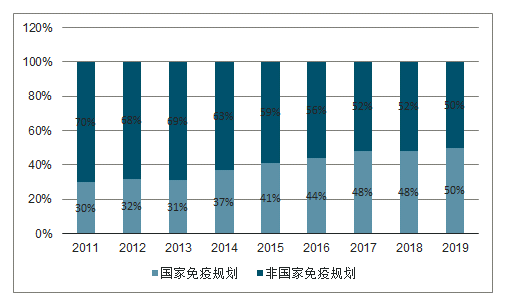
數據來源:公開資料整理
品種大類增速梳理
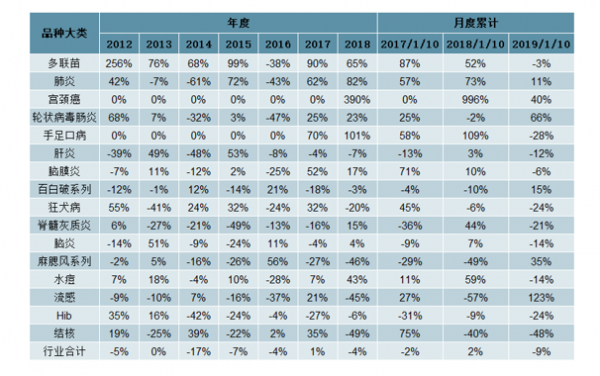
數據來源:公開資料整理
二、疫苗行業迎來發展新篇章
歷經最高立法機關三次審議,《疫苗管理法》在 2019 年 6 月 29 日獲得十三屆全國人大常委會第十一次會議表決通過,并將于 2019 年 12 月 1 日起施行。
這是我國首部有關疫苗管理的專門法律,共十一章一百條,分別對疫苗研制和注冊、疫苗生產和批簽發、疫苗流通、預防接種、異常反應監測和處理、疫苗上市后管理、保障措施、監督管理、法律責任等作出了明確規定,體現了嚴控質量、措施全面、社會共治等特點,而管得嚴、罰得重更是彰顯了我國加強疫苗監管的決心。
指明行業發展方向
《疫苗管理法》向整個疫苗行業傳遞了多方面的信息,為疫苗行業的發展指明了方向。一是嚴格準入管理。《疫苗管理法》指出,國家對疫苗生產實行嚴格的準入制度,從事疫苗生產活動,應當經省級以上人民政府藥品監督管理部門批準,取得藥品生產許可證;疫苗上市許可持有人的法定代表人、主要負責人應當具有良好的信用記錄,生產管理負責人等關鍵崗位人員應當具有相關專業背景和從業經歷。
二是社會共治。《疫苗管理法》規定了各級政府和各有關部門在疫苗的生產、流通、使用各環節中的責任;規定了新聞媒體的輿論監督責任和科學公正的報道原則;規定了疫苗產品上市許可持有人的信用公示和聯合懲戒制度;規定了疫苗生產企業的產品責任保險和異常反應補償制度;規定了監管信息和企業信息公開制度,接受社會監督等,體現了各方共同加強疫苗行業社會治理的思路。
三是嚴懲違法行為。對于違反《疫苗管理法》規定,構成犯罪的,《疫苗管理法》明確規定要“依法從重追究刑事責任”。《疫苗管理法》第八十條規定,生產、銷售的疫苗屬于假藥的,處疫苗貨值金額十五倍以上五十倍以下的罰款;生產、銷售的疫苗屬于劣藥的,處疫苗貨值金額十倍以上三十倍以下的罰款;貨值金額不足五十萬元的,均按五十萬元計算;生產、銷售的疫苗屬于假藥,或者生產、銷售的疫苗屬于劣藥且情節嚴重的,法定代表人、主要負責人等,除處所獲收入一倍以上十倍以下的罰款,終身禁止從事藥品生產經營活動外,還交由公安機關處五日以上十五日以下拘留。
四是全程監管。《疫苗管理法》從疫苗的研制、生產、流通、接種等各環節都提出了要加強監管。其中,對設備變更、工藝變更、產品質量回顧等規定了詳細的管理制度,實現疫苗全程電子追溯制度,疫苗上市許可持有人應當建立疫苗電子追溯系統,與全國疫苗電子追溯協同平臺相銜接,實現生產、流通和預防接種全過程最小包裝單位疫苗可追溯、可核查。
各方應嚴格執行法律條款
《疫苗管理法》大大強化了國家對疫苗行業的管理,勢必對整個疫苗行業造成較大影響,對行業的規范發展起到很好的助推作用。但從行業發展角度看,以下幾個方面也不容忽視。
一是提高科研創新能力。《疫苗管理法》指出,國家支持疫苗基礎研究和應用研究,促進疫苗研制和創新。我國是疫苗需求大國,疫苗在保障國人健康方面發揮著重要作用。從行業發展來看,疫苗行業始終是朝陽產業,值得相關企業大力投入。隨著我國醫改的深入進行,企業的競爭終歸要落實到創新能力上。在此背景下,疫苗上市許可持有人之間進行高水平的競爭,需要全力提升生產研發實力,尋求創新發展之路。
二是從嚴落實立法要求。疫苗上市許可持有人要從上至下把好質量關,認真落實疫苗管理的相關規定。對疫苗質量和影響最大的當屬生產環節,在日常的生產工作中,要全面貫徹實施相應的質量管理體系要求,做好質量管理工作。生產人員無疑是保證疫苗質量的最核心因素之一,對此,《疫苗管理法》在生產人員方面做了著重規定。如第二十三條規定了關鍵崗位人員備案審查制度,要求疫苗上市許可持有人的法定代表人、主要負責人應當具有良好的信用記錄,生產管理負責人、質量管理負責人等關鍵崗位人員應當具有專業背景和相關從業經歷。所以,疫苗上市許可持有人應當始終牢記人是管理環節中最重要的影響因素,嚴格執行關鍵崗位人員的準入條件,夯實疫苗安全的基礎。
三是切實加強全生命周期管理。疫苗上市許可持有人要嚴格按照行業標準實施企業的日常生產工作,勿讓類似長春長生疫苗事件再次發生。從生產到流通到貯存再到接種使用,每一個環節都要嚴格把關,不能出現任何差錯,相關企業負責人與質量負責人要承擔起相應的責任。
四是注重新科技成果的運用。《疫苗管理法》規定了對疫苗上市許可持有人的產品電子監管、產品質量監測和質量回顧分析等一系列責任,做好這些工作,離不開大數據、人工智能等新科技,所以,疫苗上市許可持有人要緊跟時代步伐,加強科技創新成果的運用,實現全程管理的信息化和智能化。保障疫苗安全,后退沒有出路,唯有和前沿科技結合才是解決之道。
五是加強行業組織建設。《疫苗管理法》既規定了政府和相關監管部門的管理責任,又強調了疫苗上市許可持有人對疫苗質量的首要責任。疫苗不安全,既要追究生產者的責任,也要追究監管者的責任。二者在法律框架內各自履行責任,但不應將二者的關系對立起來。在這個關系中,行業組織應當發揮更大的作用。普及疫苗知識,化解潛在社會風險,應當成為行業組織的重要工作內容;同時,行業組織也要成為監管部門和企業之間交流的紐帶,起到上情下達、下情上傳的作用。
總體而言,《疫苗管理法》的出臺勢必會推動整個疫苗行業的發展,對于未來,我們應抱著樂觀謹慎的態度。樂觀在于疫苗行業將迎來規范健康發展;謹慎則在于在行業規范的過程中,不可避免會遇到一些波折,而這些波折,需要行業參與者們慎重對待。
相關報告:智研咨詢發布的《2020-2026年中國動物疫苗行業投資潛力分析及投資機遇分析報告》
 智研咨詢 - 精品報告
智研咨詢 - 精品報告

2026-2032年中國多聯多價疫苗行業市場現狀調查及未來前景研判報告
《2026-2032年中國多聯多價疫苗行業市場現狀調查及未來前景研判報告》共九章,包含2021-2025年中國多聯多價疫苗行業競爭格局分析,主要多聯多價疫苗企業或品牌競爭分析,2026-2032年中國多聯多價疫苗行業發展前景預測等內容。

 公眾號
公眾號
 小程序
小程序
 微信咨詢
微信咨詢



















![研判2025!中國疫苗行業產業鏈圖譜、產業現狀、重點企業及未來前景展望:產業規模日益擴容,本土企業國際化步伐加快[圖]](http://img.chyxx.com/images/2022/0408/1ba88a0bac4b4a65439b806124f6fc0f4ab03cad.png?x-oss-process=style/w320)



