近年來政策驅動下醫藥行業正處于深刻變革進程中。一方面,受醫保控費的影響,招標、二次議價、最低價聯動、帶量采購等帶來的藥品價格壓力,特別是仿制藥的利潤率降幅較大,醫藥行業進入整體增速放緩的新常態;另一方面,隨著MAH、藥包材藥用輔料關聯審批、優先審評、eCTD等一系列政策持續推進,促使醫藥行業未來更加規范化和集中化,鼓勵創新,與國際接軌。
2018年從藥品審評來看,國務院44號、中辦國辦42號文件精神和改革措施繼續持續推進,藥品審評制度改革不斷深化,境外已上市臨床急需新藥審評加快,臨床試驗默示許可制度得到落實,原輔包與制劑實施共同審評審批,上市藥品目錄集上線運行,仿制藥質量和療效一致性評價及ICH工作繼續推進。
2016年-2019年8月創新藥NDA的申報數量
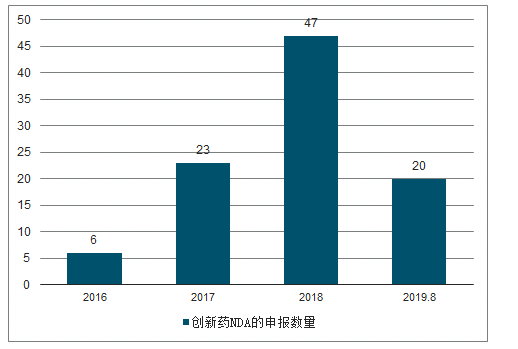
數據來源:公開資料整理
近年來國產1類化學創新藥申報情況(按品種計)
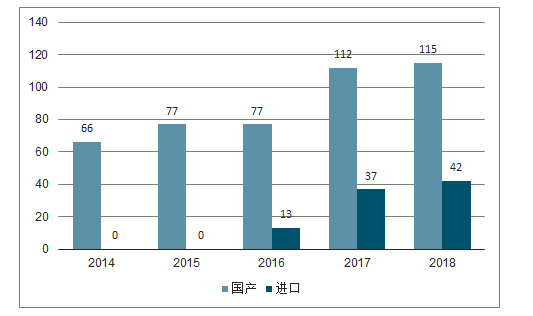
數據來源:公開資料整理
在藥品注冊申請積壓情況改善、政府鼓勵藥品創新的背景下,從2016年起,藥品研發的申報數量從臨床核查后的低谷逐步回升,2018年化藥、生物制品、中藥的申報數量都創了2016年以來的新高。
2009-2018年各年度CDE受理審評數量
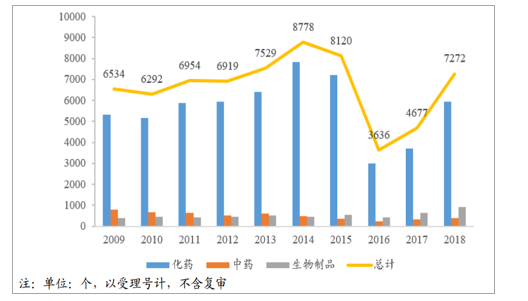
數據來源:公開資料整理
近年來國內創新藥獲批情況
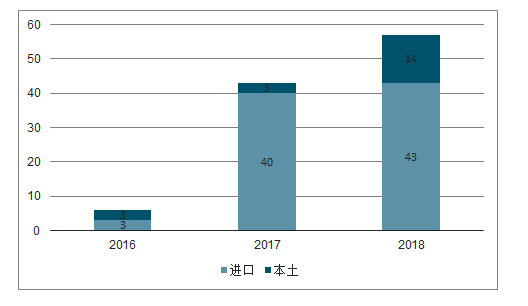
數據來源:公開資料整理
2018年7月至今國內外主要醫藥企業獲得默許許可開展臨床試驗數量
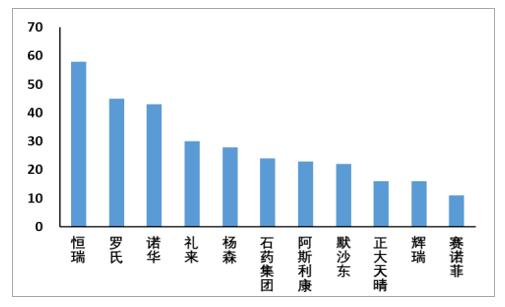
數據來源:公開資料整理
中國創新藥市場空間測算
2018年中國創新藥(以化藥、生物藥為主)銷售額占所有藥物比例約為2.5%,占非中藥比例為4.17%,遠低于美國和日本的水平。我們預計到2024年,中國創新藥銷售額占非中藥的比例有望達到10%,2029年有望達到30%。創新藥銷售額有望達到7000億元以上,年復合增速近30%。
中國各類藥品銷售額預測(單位:億元)
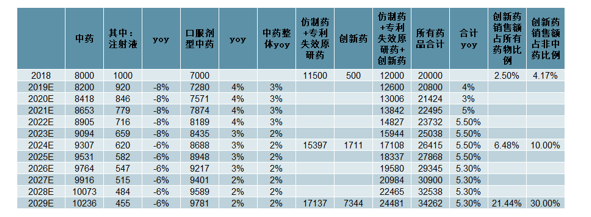
數據來源:公開資料整理
相關報告:智研咨詢發布的《2020-2026年中國創新藥行業市場現狀調研及投資機會預測報告》

 公眾號
公眾號
 小程序
小程序
 微信咨詢
微信咨詢


















![2026年中國合成生物行業發展全景分析:下游應用從醫藥健康、化工材料向農業食品、能源環保全面滲透,行業已展現出巨大的應用潛力[圖]](http://img.chyxx.com/images/2022/0408/55d853aceb464ffcf6fad7c27bbd7795797b1b5a.png?x-oss-process=style/w320)
![2026年中國骨密度儀行業產業鏈圖譜、采購總量、采購金額、獲批企業、競爭格局及未來競爭趨勢分析:外資品牌占據主導地位[圖]](http://img.chyxx.com/images/2022/0330/e060dd24be7392f76ddd0a84489963879d953ac6.png?x-oss-process=style/w320)
![研判2026!中國物聯網行業概念、市場規模、企業競爭格局分析:中國物聯網產業領跑全球,AI融合驅動“泛在智聯”新紀元[圖]](http://img.chyxx.com/images/2022/0330/ce25a2275c336b52d58303ed80fb7924b3fd1022.png?x-oss-process=style/w320)
![研判2026!中國汽車行業分類、產銷量、重點企業銷量分析:一季度中國汽車行業現“內冷外熱”分化,出口同比激增成核心增量引擎[圖]](http://img.chyxx.com/images/2022/0330/ff5315f651f3e124d0f5a156ac51655e46e5433f.png?x-oss-process=style/w320)
![2026年中國彩鋼板行業發展歷程、供需情況、市場規模、競爭格局及趨勢研判:彩鋼板市場規模達1138.76億元,鋼結構與綠色建材政策驅動增長[圖]](http://img.chyxx.com/images/2022/0330/4279f04d08c7260a105d321a303d34a91af3a3d5.png?x-oss-process=style/w320)
![2026年中國UV燈管行業產業鏈、發展現狀、競爭格局、競爭趨勢分析:外資壟斷高端賽道,中低端市場競爭白熱化[圖]](http://img.chyxx.com/images/2022/0330/b388a599ab8b82a70e79838a8b0d600efa11727f.png?x-oss-process=style/w320)
