生物醫藥外包包括:研發外包(CRO)、生產外包(CMO)、銷售外包(CSO)、管理外包(SMO)及其他外包服務,最主要的還是CRO與CMO。
與全球CRO市場以臨床前研究為主不一樣的是,目前國內CRO公司業務主要集中在新藥早期臨床前研發以及臨床研究兩大方面,其中臨床前研究約占43%;臨床試驗研究約占57%。2018年我國臨床前研究市場規模為268.3億元;臨床試驗研究市場規模為360億元。
2007-2018年中國CRO細分市場收入
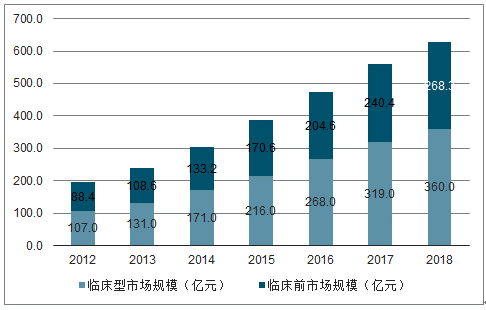
數據來源:公開資料整理
2018年中國CRO市場結構占比
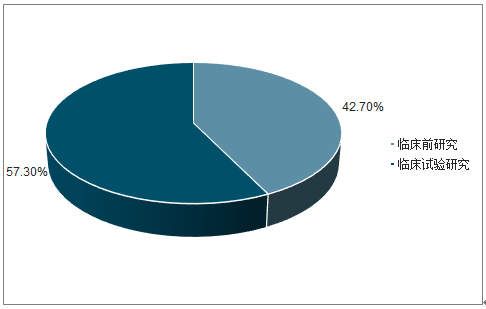
數據來源:公開資料整理
一、醫藥外包服務(CRO/CMO):政策催化行業高景氣
從CDE公布的歷年藥品審評報告可以看出,從2015年起,我國藥品注冊申請審評審批(包括臨床試驗申請、進口再注冊申請、補充申請、ANDA、NDA等)速度明顯加快,從2015年前的年均5000件審評完結量大幅提升到1萬件左右;CDE藥品注冊審評大幅提速,積累等待審評量從2015年高峰期20000萬件下降到2017年末約4000件水平,2018年新增新藥注冊受理數量回升,年末積累等待評審數量小幅回升到4370件左右。評審速度翻倍,新藥審批等待時間大幅縮減,都有利于CRO行業潛在客戶需求提升。
CDE新藥注冊審評審批完結量和積累量(件)
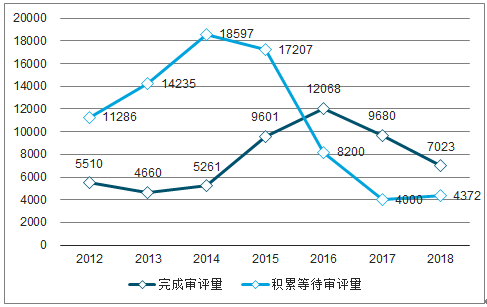
數據來源:公開資料整理
從2012年開始,國務院和藥監部門就提出開展仿制藥一致性評價,2016年3月,國務院辦公廳正式對外公布《關于開展仿制藥質量和療效一致性評價的意見》,規定化學藥品新注冊分類實施前批準上市的仿制藥,凡未按照與原研藥品質量和療效一致原則審批的,均須開展一致性評價。仿制藥一致性評價包括藥學等效(PE)和生物等效(BE)兩部分,國家基藥目錄289個品種需要在2018年底完成,我國大部分藥企不具備資源自行開展一致性評價的能力,大型藥企有自行開展能力但是旗下擁有批文眾多,時間就是金錢,誰先通過一致性評價,誰將搶占一致性評價后藥品市場。
2017年一致性評價收入大幅提升到1.81億元,同比大增190%,營收占比提升到10.7%;2018全年完成約100個一致性評價項目,營收超3億元。
二、國際CRO向國內產業轉移:低成本、龐大人口和豐富疾病譜
低成本、龐大人口和豐富疾病譜,促使國際CRO向國內產業轉移。目前,新藥研發難度不斷提高,高投入、長周期、高淘汰率始終伴隨新藥研發全過程;另外,藥企現有專利藥將在未來幾年內專利保護集中到期,專利懸崖導致仿制藥沖擊專利藥原有市場,降價和市場被蠶食不可避免。國際藥企為降本增效,有動力在持續高投入新藥研發的基礎上,尋求低成本的各類醫藥外包服務,國際新藥研發CRO正在經歷向包括中國在內的亞洲低成本地區轉移浪潮,主要基于以下幾點:低成本。具體體現在高素質低成本的專業人才獲取和低成本的臨床病例兩方面。
高素質低成本的專業人才。每年我國大學高校畢業人數超過700萬,碩博研究生招生人數超過60萬,擁有大量后備專業人才儲備;另外,海外有豐富從業經驗的各類醫藥外包服務人才回流國內。我國人均收入水平遠低于歐美發達國家,高素質低成本的專業人才獲取,為人才與技術密集型的我國CRO行業帶來競爭優勢。
低成本的臨床病例。國外對藥物在人體進行試驗管理相當嚴格,藥物觀察和注冊周期都很長,對試藥人有嚴格保護措施;另外,國內外平均收入差距巨大,我國受試人獲得的經濟補償只有美國的1/10。據調查數據顯示,將各類藥物的臨床試驗數據平均來看,2010年在美國完成1例Ⅰ期臨床試驗所需的綜合成本約為6000美元,Ⅱ期臨床試驗為7000美元,Ⅲ期臨床試驗為8000美元。在中國進行臨床試驗完成一例合格病例所需的成本通常不超過20000元,大大低于國外的試驗成本。國內低廉的研究成本吸引海外訂單轉移。
龐大的病患人群和豐富的疾病譜。我國人口眾多,在疾病種類的多樣性和病例數量方面擁有其他國家所不具備的條件,足夠數量臨床試驗病例的召集和臨床終點的完成,相比歐美發達國家都有優勢,尤其是在一些罕見病或需要長時間臨床終點的癌癥等疾病方面,可入列臨床病例數大大提高,提高了臨床試驗研究的可靠性和統計學意義。
國內外臨床試驗成本比較(單位:美元)
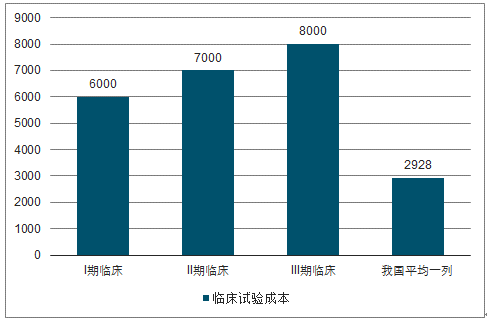
數據來源:公開資料整理
醫藥外包服務(CRO/CMO)行業上市公司主要有藥明康德、泰格醫藥、康龍化成、博濟醫藥、昭衍新藥、凱萊英和百花村,百花村由于計提資產減值,導致2017-2018年連續兩年扣非凈利潤重大虧損。近年來,醫藥外包服務行業受鼓勵藥械創新和仿制藥一致性評價政策影響,營收連年實現快速增長,2018年,行業主要公司營收均實現20%以上的高增長;扣非后核心凈利潤方面,均實現24%以上高速增長,利潤增速高于營收增速,頭部企業2019年估值水平在45倍左右,成長性和估值相對匹配。
醫藥外包服務CRO/CMO仍將快速增長,標的上選擇行業頭部公司,如藥明康德、泰格醫藥、康龍化成。藥明康德是一家覆蓋新藥研發、生產全流程的CRO/CMO企業,優勢在CRO上游新藥分子開發和篩選以及CMO領域,近年來也逐步拓展臨床CRO業務,以實現CRO、CMO全覆蓋;泰格醫藥主要集中在臨床CRO;康龍化成優勢在上游新藥分子開發和篩選,在國內新藥分子發現領域營收僅次于藥明康德,近年來逐漸向臨床CRO、CMC等全產業鏈拓展。
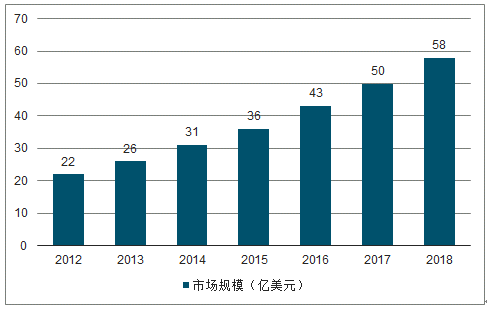
2012年中國CMO市場容量為22億美元,同比增長16%,而2018年其增長將超過2012年一倍多,達到58億美元,5年的CAGR為17.62%。由于政策所限,目前大部分國內CMO只能開發國際市場,主要客戶是國際制藥巨頭,隨著國內市場的逐步開啟,國內CMO增速有望繼續突破。
2012-2018年中國CMO市場規模趨勢
數據來源:公開資料整理
而在醫藥外包方面,中國醫藥服務外包市場潛力無限。特別近幾年,中國加速推行醫藥體制改革,國家已經明確把醫藥產業作為一個新興產業進行推動,并加大投資力度。中國已經成為全球最具吸引力的醫藥投資市場,越來越多的外資企業來到中國,挖掘市場商機和尋找合作伙伴。
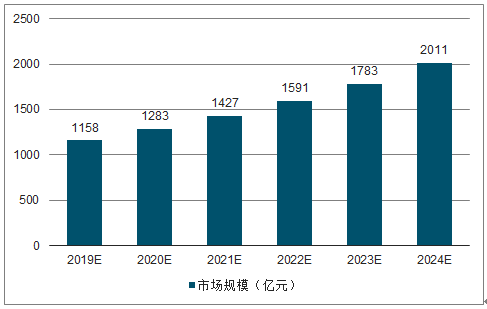
目前中國生物醫藥外包服務企業近千家,藥物研究開發生產外包服務市場規模達超過千億規模,隨著我國醫藥行業以及服務外包行業利好政策不斷,我國醫藥外包行業將會繼續保持較高速度增長,未來5年藥物研究開發生產外包服務市場規模將保持10%-15%的增速,預計2024年我國藥物研究開發生產外包服務市場規模將達2000億元以上。
2019-2024年中國藥物研究開發生產外包服務市場規模及預測
數據來源:公開資料整理
相關報告:智研咨詢發布的《2019-2025年中國CRO醫藥研發外包行業運營態勢及投資前景預測報告》
 智研咨詢 - 精品報告
智研咨詢 - 精品報告

2026-2032年中國醫藥外包(CXO)行業市場運營態勢及投資機會研判報告
《2026-2032年中國醫藥外包(CXO)行業市場運營態勢及投資機會研判報告》共十一章,包含中國醫藥外包(CXO)行業重點企業布局案例研究,中國醫藥外包(CXO)行業市場前景預測及發展趨勢預判,中國醫藥外包(CXO)行業投資戰略規劃策略及建議等內容。

 公眾號
公眾號
 小程序
小程序
 微信咨詢
微信咨詢


















![2026年中國醫藥外包(CXO)?行業政策、運行現狀、細分市場、競爭格局及未來發展趨勢研判:創新藥融資與BD交易雙升,CXO行業景氣度持續向上[圖]](http://img.chyxx.com/images/2022/0408/54b870b64f647f1fc10474b02796382c9242dcfa.png?x-oss-process=style/w320)

![智研研判!醫藥制造外包(CMO/CDMO)行業現狀及趨勢分析:國產企業加速拓展高附加值業務,行業規模不斷擴容[圖]](http://img.chyxx.com/images/2022/0408/55d853aceb464ffcf6fad7c27bbd7795797b1b5a.png?x-oss-process=style/w320)


