一、從全球市場份額來看,中國有巨大的上升空間及承接實力
全球CXO企業同中國企業收入差距巨大,國內具備誕生超大企業潛力:全球CRO排名第一的LabCorp2018年收入達到113億美元,而國內最大的藥明康德收入僅為14億美元,在全球產業向中國轉移的大背景下,國內市場具備超大企業潛力。
從全球市場份額來看,中國有巨大的上升空間及承接實力:中國擁有工程師紅利,研發和運營成本遠低于歐美發達市場,同時也掌握了藥物研發生產環節的核心技術,從而引導CRO、CDMO產業轉移至國內。從2017年來看,中國CRO行業僅占全球CRO行業18.6%的市場份額,CMO更是僅有7.8%的市場份額,未來仍有巨大的可提升空間。
全球CRO、CMO市場規模及增速(億美元)

數據來源:公開資料整理
相關報告:智研咨詢發布的《2019-2025年中國CRO行業市場專項調研及投資前景預測報告》
全球CXO企業同中國企業收入差距巨大,國內具備誕生超大企業潛力:全球CRO排名第一的LabCorp2018年收入達到113億美元,而國內最大的藥明康德收入僅為14億美元,在全球產業向中國轉移的大背景下,國內市場具備超大企業潛力。
從全球市場份額來看,中國有巨大的上升空間及承接實力:中國擁有工程師紅利,研發和運營成本遠低于歐美發達市場,同時也掌握了藥物研發生產環節的核心技術,從而引導CRO、CDMO產業轉移至國內。從2017年來看,中國CRO行業僅占全球CRO行業18.6%的市場份額,CMO更是僅有7.8%的市場份額,未來仍有巨大的可提升空間。
國內CRO、CMO全球市場份額占比
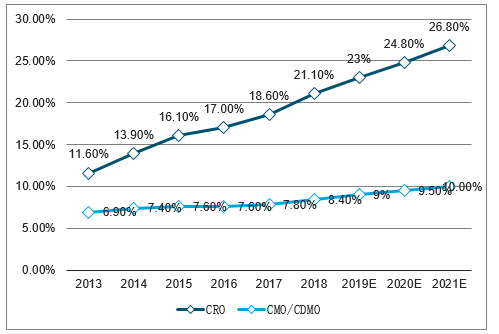
數據來源:公開資料整理
四大變化促進國內CXO行業迎來歷史性戰略機遇,產業轉移+政策鼓勵+科創板帶動+創新產品進入到收獲期:(1)全球產能轉移大背景下,國內政策進一步推動產業發展:包括審評審批加速,醫保談判準入,上市許可人制度、新化藥注冊分類在內的一系列創新藥配套政策推動國內醫藥產業由“仿制驅動”上升至“創新驅動”,兩辦發布“國36條”更是將創新上升至國家高度,將對前端的創新產業鏈服務商帶來國內市場新增量。(2)科創板的即將推出,也開拓創新藥融資新渠道:一級市場退出機制更加多樣化,將鼓勵其投資創新藥項目,同時傳統藥企向創新藥企戰略轉型的自身代價更低,新藥申報數量將快速增加,長期有利于行業發展。
對于創新藥服務商來說,醫藥產業研發動力的增強將直接轉換為未來市場規模的增長以及業績的兌現。推薦重點關注凱萊英、昭衍新藥、藥石科技、藥明康德、泰格醫藥、康龍化成,二線如博騰股份、九州藥業、量子生物等、其他創新藥服務商艾德生物等。
二、醫療外包:看好訂單充沛、業績能見度高的行業領先者
國內醫藥外包行業持續高景氣:1)2017年中國CRO市場規模為559億元,2013-2017年復合增速為24.4%;2)2017年中國CMO市場規模為314億元,2013-2017年復合增速為17.9%。
2012-2021E年國內CRO市場規模及增速

數據來源:公開資料整理
2012-2021E年國內CMO市場規模及增速
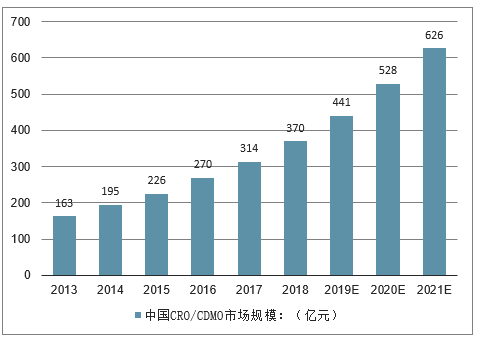
數據來源:公開資料整理
三、國內醫藥外包市場中長期驅動因素如下
1)政策利好創新,推動醫藥外包市場擴容。國家近年鼓勵創新,發布多項文件加速優先審評、藥品上市許可持有人制度(MAH)等政策落地,利好醫藥外包市場擴容。
2015年至今國家鼓勵藥品創新及MAH政策匯總
時間 | 部門 | 政策或事件 | 主要內容 |
2015.8 | 國務院 | 《關于改革藥品醫療器械審評審批制度的意見》 | 優化藥品審評審批流程,加快藥品審評審批速度 |
2017.6 | ICH | 中國成為ICH(人用藥物注冊技術要求國際協調會)成員 | CFDA正式與國際標準接軌,參與到全球的藥品審批和監管體系,有助于促進中國藥物研發的創新,提高藥品質量和標準 |
2017.8 | CFDA | 《關于推進藥品上市許可持有人制度(MAH)試點工作有關事項的通知》 | 藥品的所有者與生產者得以合法分離,持有藥品上市許可的企業可以自行生產,也可將產品委托給具備GMP條件的生產商生產 |
2017.10 | 國務院 | 《關于深化審評審批制度改革鼓勵藥品醫療器械創新的意見》 | 鼓勵支持中國創新藥品和器械的發展 |
2017.12 | CFDA | 《關于鼓勵藥品創新實行優先審評審批的意見》 | 明確了優先審評審批的范圍、程序和工作要求 |
數據來源:公開資料整理
2)低成本優勢促進訂單跨境轉移,中國有望優先獲益。相比西方發達國家,我國醫藥企業在研發生產上具有明顯成本優勢(低約30%-60%),有望促進醫藥外包訂單跨境轉移。
中國醫藥研發生產具有成本優勢

數據來源:公開資料整理
3)國內創新產業的崛起。從“metoo”到“mebetter”,再到“best/firstinclass”,我國的醫藥創新已經迎來了嶄新的時代,恒瑞醫藥、石藥集團、百濟神州等公司通過研發構建了強大的研發管線,為國內外包市場帶來新增量。
 智研咨詢 - 精品報告
智研咨詢 - 精品報告

2026-2032年中國CRO行業市場全景評估及發展策略分析報告
《2026-2032年中國CRO行業市場全景評估及發展策略分析報告》共十四章,包含中國CRO(醫藥研發合同外包服務行業領先企業競爭力分析,2026-2032年中國CRO(醫藥研發合同外包服務)行業發展趨勢與前景分析,研究結論及建議等內容。

 公眾號
公眾號
 小程序
小程序
 微信咨詢
微信咨詢



















![研判2024!中國醫藥研發外包(CRO)行業發展歷程、產業鏈、市場規模及未來前景分析:國內醫藥創新研發需求日益增長,醫藥外包市場規模加速擴容[圖]](http://img.chyxx.com/images/2022/0330/ce25a2275c336b52d58303ed80fb7924b3fd1022.png?x-oss-process=style/w320)
![2022年中國CRO行業發展前景分析:受益于醫藥創新和數字化轉型,行業將繼續保持增長勢頭[圖]](http://img.chyxx.com/images/2022/0330/920e1a3ff3bb6b7f469fbaa1e9ad45bc470a7578.png?x-oss-process=style/w320)
![2022年中國CRO行業全景速覽:CRO行業發展進入快車道[圖]](http://img.chyxx.com/images/2022/0330/6b296592ed87ae76d174b4fbc262ff18a3c189b8.png?x-oss-process=style/w320)

![藥明康德2021年業績預告發布!實現營收229.02億元,CRDMO帶動業績高速增長[圖]](http://img.chyxx.com/2022/02/K8532W8O9B_m.png?x-oss-process=style/w320)
