現階段,受各渠道化學致癌因素的增加,不良生活習慣導致免疫力低下及環境污染加劇等內外因共同作用下,全球范圍內癌癥患病率和發病率都有不同程度的提升。各國相關藥品研發生產企業根據市場需求的變動也迅速做出反應,增加對腫瘤藥的研發,而美國食品藥品監督管理總局FDA也根據實際情況增加了對抗腫瘤藥審批的關注。
免疫治療藥物,如靶向PD-1/PD-L1或CTLA-4的藥物,以及第一個獲得FDA批準的用于癌癥治療的病毒療法T-VEC,對晚期黑色素瘤患者的生存有著顯著的影響。2001年的一項研究計算出,確診后10年的存活率低于10%,但現在很大程度上要歸功于這些免疫療法,存活率飆升至50%以上。
然而,免疫治療一些患者對完全不起作用,盡管研究人員已經開始尋找證據來解釋其中的原因,最近的研究表明,DNA突變較多的腫瘤更有可能有反應,但這可能不是一個單一的原因,而是多種因素組合的結果。
從獲得審批的具體新藥請情況看,2018年FDA新藥評審中心(CDER)共批準了59個新藥,其中新分子實體42個,生物制品17個,該數據打破了1996年批準53個新藥的紀錄。
從獲批新藥的治療領域看,抗腫瘤新藥是目前重要的關注領域。除2016年抗腫瘤新藥獲批數量僅為5種外,從2014年起FDA通過腫瘤新藥數量呈穩步上升趨勢;2018年FDA通過的16種腫瘤新藥中,治療實體腫瘤新藥的比例超過50%。
2010-2018年FDA每年批準新藥數量和腫瘤新藥數量:種
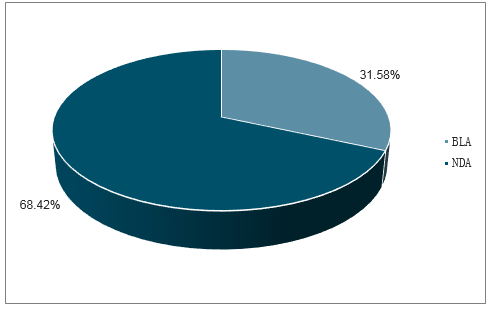
數據來源:公開資料整理
相關報告:智研咨詢發布的《2019-2025年中國中藥抗腫瘤藥物行業市場全景評估及發展趨勢預測研究報告》
2014-2018年FDA通過的腫瘤藥物分類占比圖顯示,2016年后FDA對腫瘤藥物的審批越來越關注非實體瘤領域。2018年,FDA批準的腫瘤新藥中,治療實體瘤新藥有9種,占比56.25%,非實體瘤藥物7種,占比43.75%,基本持平。
2014-2018年FDA每年批準抗腫瘤新藥分類%
數據來源:公開資料整理
2018年59種新藥批準中,43種(73%)被指定為四種審評方式種的一個或多個類別,其中優先審查24種(41%),14種(24%)為突破性療法,43種(73%)為優先審查,4種(7%)加速批準。
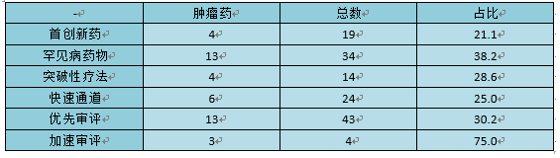
從獲批抗腫瘤藥不同審批方法看,首創型腫瘤藥4中,罕見病腫瘤藥物13種。都是該審批方法中占有較高比例的獲批新藥。除此之外,有13種抗腫瘤藥獲得優先審批,占比30.2%。在全年4個獲得加速審批通過的新藥中,其中3個都為腫瘤藥物。由此可見腫瘤藥的審批獲得FDA的重點關注。
2018年FDA腫瘤藥物獲批情況

數據來源:公開資料整理
腫瘤,由于其種類眾多、致病原因不一、復發率高,成為長期困擾人們的疾病之一。近年來,FDA對腫瘤藥物的批準呈穩步上升趨勢。在2018年FDA發布的《報告》中,FDA共批準了腫瘤新藥和腫瘤類似生物藥19個。其中腫瘤新藥16種,以美國企業申請為主,白血病為獲批藥品的重要關注領域,其大多處在臨床III期。而腫瘤生物類似藥品3種,多為美國FDA生物制品許可申請為主。
從獲批腫瘤藥不同的終點情況看,主要表現為臨床II期、臨床III期,其中基于臨床Ⅱ期獲批的有7種,占比36.8%;基于臨床Ⅲ期獲批的有8種,占比42.1%;基于等效臨床表現評價獲批的生物類似藥有2種,占比10.6%。除此之外,基于臨床Ⅰ期和基于新型終點MFS獲批的新藥均為1種,占比5.3%。
2018年美國FDA腫瘤藥獲批終點結構
數據來源:公開資料整理
從獲批抗腫瘤新藥的申請單位看,美國藥企為主要的申請單位,以ARRAY、VERASTEM、輝瑞和強生等美國著名的藥品生產企業為代表。2018年獲得FDA批準的16個腫瘤新藥+3個腫瘤生物類似藥品中,美國本土品牌申請數量為14個,遙遙領先。法國、日本和瑞士企業申請成功的抗腫瘤藥品數量分別為2個和1個。
2018年美國FDA分國家腫瘤藥獲批情況統計(種)

數據來源:公開資料整理
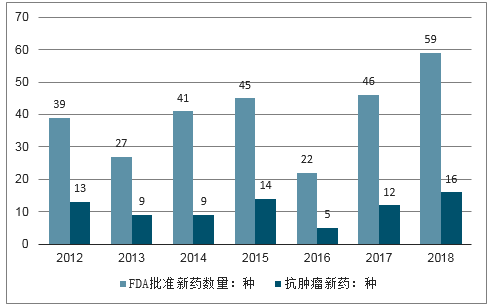
美國FDA審批通過的抗腫瘤藥主要分為新藥申請(NDA)和生物制品許可藥(BLA)兩種,其中NDA為抗腫瘤藥的主要產品類型。2018年獲批的19種抗腫瘤相關藥品中,NDA抗腫瘤藥為13種,占獲批藥品數量的68.42%;BLA藥品6種,占比31.58%。
2018年美國FDA分品類腫瘤藥獲批情況統計

數據來源:公開資料整理

 公眾號
公眾號
 小程序
小程序
 微信咨詢
微信咨詢

















![趨勢研判!2024年中國腫瘤治療藥物行業產業鏈、發展現狀及競爭格局分析:癌癥發病例數不斷增加,抗腫瘤藥物市場規模持續上漲[圖]](http://img.chyxx.com/images/2022/0330/ce25a2275c336b52d58303ed80fb7924b3fd1022.png?x-oss-process=style/w320)
![趨勢研判!2026年中國浮選藥劑行業發展歷程、產業鏈、市場規模、競爭格局、重點企業及發展趨勢:市場規模持續增長,行業呈現高度分散的競爭格局[圖]](http://img.chyxx.com/images/2022/0408/55d853aceb464ffcf6fad7c27bbd7795797b1b5a.png?x-oss-process=style/w320)
![研判2026!中國二氧化碳行業分類、產業鏈、價格及重點企業分析:從工業氣體到碳循環樞紐,二氧化碳從“末端治理”邁向“資源化利用”[圖]](http://img.chyxx.com/images/2022/0330/99d4e8a78387e45474dcca8da0b56041c69dec09.png?x-oss-process=style/w320)
![研判2026!中國城市軌道交通運維檢修行業市場政策、產業鏈、市場規模、競爭格局及未來發展趨勢分析:央企及其子公司占據主導地位[圖]](http://img.chyxx.com/images/2022/0408/54b870b64f647f1fc10474b02796382c9242dcfa.png?x-oss-process=style/w320)
![2026年中國水性色漿行業產業鏈、發展現狀、競爭格局、競爭趨勢分析:國際巨頭把持高端技術,國內企業加速規模擴張與行業整合[圖]](http://img.chyxx.com/images/2022/0330/b388a599ab8b82a70e79838a8b0d600efa11727f.png?x-oss-process=style/w320)
